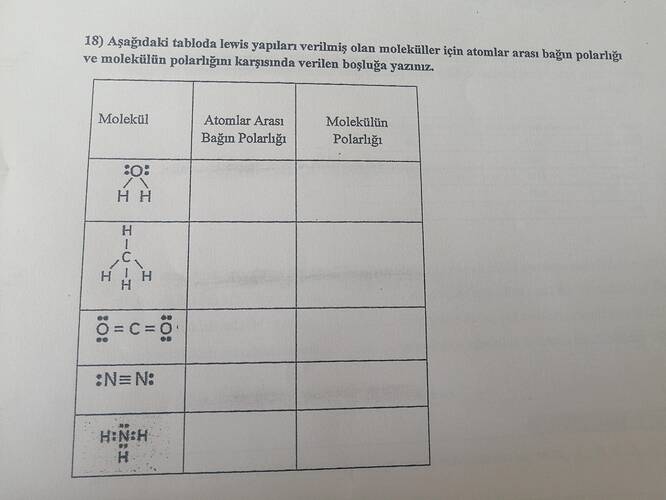
18) Aşağıdaki tabloda Lewis yapıları verilmiş olan moleküller için atomlar arası bağın polarlığı ve molekülün polarlığını karşısında verilen boşluğa yazınız.
Answer:
Adım Adım Çözüm
-
H₂O (Su) Molekülü
- Lewis yapısında merkezde O atomu, iki yanında H atomları ve iki yalnız (bağımsız) elektron çifti bulunur.
- Atomlar Arası Bağ Polarlığı: O–H bağları elektronegatiflik farkı nedeniyle polardır (Oksijen, Hidrojenden daha elektronegatif).
- Molekülün Polarlığı: Molekül bükük (V şekilli) bir yapıdadır ve dipol momentleri birbirlerini sıfırlamaz. Bu nedenle molekülü de polardır.
-
CH₄ (Metan) Molekülü
- Lewis yapısında merkezde C atomu, etrafında bağ yapmış dört H atomu vardır.
- Atomlar Arası Bağ Polarlığı: Karbon ile hidrojen arasındaki elektronegatiflik farkı çok az olduğu için C–H bağları göreceli olarak zayıf polarlığa sahiptir. Genellikle lise seviyesinde bu bağlar “nonpolar” veya çok düşük polarlık kabul edilir.
- Molekülün Polarlığı: Yapı tetrahedral ve simetrik olduğu için dipol momentleri birbirini sıfırlar; dolayısıyla molekül nonpolardır.
-
CO₂ (Karbon Dioksit) Molekülü
- Lewis yapısında merkezde C, her iki tarafta O atomu ve aralarında çift bağlar bulunur (O=C=O).
- Atomlar Arası Bağ Polarlığı: C=O bağları polardır (Oksijenin elektronegatifliği Karbondan yüksektir).
- Molekülün Polarlığı: Molekül doğrusal (linear) yapıdadır. İki kutuplu bağ birbirine zıt yöndedir, bu yüzden toplam dipol momenti sıfırlanır. Molekül nonpolardır.
-
N₂ (Azot) Molekülü
- Lewis yapısında iki N atomu arasında üçlü bağ (N≡N) bulunur.
- Atomlar Arası Bağ Polarlığı: İki aynı atomun oluşturduğu bağda elektronegatiflik farkı 0 olduğu için nonpolardır.
- Molekülün Polarlığı: İki atomdan oluştuğu ve aynı element olduğu için molekül de nonpolardır.
-
NH₃ (Amonyak) Molekülü
- Lewis yapısında merkezde N atomu, üç hidrojenle bağ yapar ve bir çift yalnız (bağımsız) elektron bulunur.
- Atomlar Arası Bağ Polarlığı: N–H bağları polardır (Azot, Hidrojenden daha elektronegatif).
- Molekülün Polarlığı: Molekül trigonal piramit (üçgen piramit) şeklindedir ve asimetriktir. Dipol momentleri birbirini sıfırlayamadığından molekül polardır.
Özet Tablo
| Molekül | Atomlar Arası Bağ Polarlığı | Molekül Polarlığı |
|---|---|---|
| H₂O | O–H bağı polardır | Polar |
| CH₄ | C–H bağı çok düşük polar veya nonpolar kabul edilir | Nonpolar |
| CO₂ | C=O bağı polardır | Nonpolar |
| N₂ | N≡N bağı nonpolardır | Nonpolar |
| NH₃ | N–H bağı polardır | Polar |
Kısa Özet:
• H₂O ve NH₃, merkez atomları üzerindeki yalnız elektron çiftlerinin oluşturduğu asimetrik yapıları nedeniyle polar moleküllerdir.
• CH₄ molekülü dört simetrik C–H bağı içerir ve nonpolar moleküldür.
• CO₂’de bağlar polar olsa da molekül doğrusal olduğu için net dipol momenti sıfırlanır ve molekül nonpolardır.
• N₂ molekülünde aynı atomlar arasındaki üçlü bağ nonpolardır ve molekül de nonpolardır.