Soru: Aşağıda verilen moleküllerin Lewis yapısını göstererek, molekülün polar olup olmadığını belirtiniz. (Örnek: H₂, O₂, BF₃)
Cevap:
Bu tip sorularda öncelikle her molekülün Lewis yapısını çizer, ardından molekülün şeklini (geometrisini) belirleyerek polar mı yoksa apolar (non-polar) mı olduğuna karar veririz. Aşağıdaki özet tablo ve açıklamalar, H₂, O₂ ve BF₃ moleküllerinin Lewis yapıları, molekül geometrileri ve polarlıkları hakkındaki temel bilgileri sunmaktadır.
| Molekül | Lewis Yapısı | Molekül Geometrisi | Hibritleşme | Bağ Açısı | Polarlık |
|---|---|---|---|---|---|
| H₂ | H – H | Doğrusal (2 atomlu) | Yok (s orbital) | Yaklaşık 180° | Apolar |
| O₂ | O=O (her O’da 2 çift elektron) | Doğrusal (2 atomlu) | Yok (p orbitalleri) | Yaklaşık 180° | Apolar |
| BF₃ | F F \ / B \ / F (Her F’de 3 çift elektron) |
Üçgen Düzlem (Trigonal Planar) | sp² | Yaklaşık 120° | Apolar (Simetrik) |
-
H₂ (Hidrojen) Molekülü
- Lewis Yapısı: Her bir H atomu tek elektrona sahiptir ve iki H arasındaki tekli kovalent bağ ile oktet (hidrojende dublet) kuralı sağlanır.
- Geometri: İki atomlu moleküller doğrusaldır.
- Polarlık: İki aynı atomun oluşturduğu moleküllerde elektron bulutu eşit paylaşıldığından net dipol momenti yoktur; bu nedenle H₂ apolardır.
-
O₂ (Oksijen) Molekülü
- Lewis Yapısı: İki O atomu arasında çifte (ikili) bağ bulunur. Her O atomunda 2’şer tane bağlanmamış elektron çifti (lone pair) vardır.
- Geometri: İki atomlu olduğu için doğrusaldır.
- Polarlık: İki aynı atom elektronları eşit olarak paylaştığı için net dipol momenti sıfırdır; dolayısıyla O₂ apolardır.
-
BF₃ (Bor Triflorür)
- Lewis Yapısı: Bor, merkez atom olup 3 adet flor atomu ile tekli kovalent bağ yapar. Her fluor atomu 3 çift bağlanmamış elektrona (lone pair) sahiptir.
- Geometri: Üçgen düzlem (trigonal planar). Bor atomu genellikle oktet kuralını tam doldurmaz; 6 değerlik elektronu vardır.
- Polarlık: Geometri simetriktir (120°’lik açıyla yayılmış üç F). Her B–F bağı polar olsa da vektörel olarak birbirlerini götürdükleri için BF₃’ün net dipol momenti sıfırdır, yani apolar bir moleküldür.
Bu bilgiler doğrultusunda, H₂ ve O₂’nin hem aynı tür atomlar içermeleri hem de doğrusal yapılarından dolayı apolar, BF₃’nin ise üçgen düzlemdeki simetrik yapısından ötürü apolar olduğu unutulmamalıdır.
Soru: H₂O, PCl₃, CCl₄, CO₂, CH₃Cl ve C₂H₆ moleküllerinin polarlıklarını (polar-apolar) belirtiniz.
Cevap:
Aşağıdaki tabloda bu moleküllerin Lewis yapıları, geometrileri ve polarlıkları özetlenmiştir. Moleküllerin polarlığını belirlemenin en temel yolu, molekülün geometrik şeklini ve bağ içi elektronların dağılımını (elektronegatiflik farklarını) incelemektir.
| Molekül | Lewis Yapısı Özet | Molekül Geometrisi | Bağ Açıları (°) | Polarlık |
|---|---|---|---|---|
| H₂O | O merkez atom, 2 H bağlanmış, 2 lone pair | Bükük (Bent) | ~104.5° | Polar |
| PCl₃ | P merkez atom, 3 Cl bağlanmış, 1 lone pair | Üçgen Piramidal (Trigonal Pyramidal) | ~107° | Polar |
| CCl₄ | C merkez atom, 4 Cl bağlanmış, lone pair yok | Tetrahedral | ~109.5° | Apolar |
| CO₂ | C merkez atom, 2 O bağlanmış, bağlar çiftli (C=O) | Doğrusal (Linear) | 180° | Apolar |
| CH₃Cl | C merkez atom, 3 H + 1 Cl bağlanmış, lone pair yok | Tetrahedral | ~109.5° | Polar |
| C₂H₆ | Her C atomu, 3 H bağlanmış ve 1 C ile bağ yapmış (toplam 4 bağ) | Her C etrafı Tetrahedral | ~109.5° | Apolar |
Kısa Açıklamalar
-
H₂O (Su):
- Oksijenin yüksek elektronegatifliği ve bükük (V şeklinde) geometri nedeniyle dipol momenti sıfırlanmaz; molekül polardır.
-
PCl₃ (Fosfor Trişlorür):
- Merkezde 1 tane bağlanmamış elektron çifti (lone pair) bulunur. Üçgen piramidal yapı, bağların vektörel toplamını yok etmez ve P–Cl bağları polardır. Bu nedenle polardır.
-
CCl₄ (Karbon Tetra klorür):
- Tetrahedral geometri içerisinde dört kutuplu C–Cl bağları birbirini simetrik olarak dengeler; net dipol momenti sıfırdır, dolayısıyla apolardır.
-
CO₂ (Karbon Dioksit):
- Doğrusal (linear) yapıda iki C=O bağı karşılıklı olarak birbirini dengeler, net dipol momenti oluşmaz; apolardır.
-
CH₃Cl (Klorometan):
- Tetrahedral yapıda tek klor atomunun elektronegatifliği daha yüksek olduğu için negatif yük Cl tarafında yoğunlaşır ve H’ler tarafından dengelenemez, bu nedenle polardır.
-
C₂H₆ (Etan):
- Her iki Karbon da tetrahedral bir düzen içerisindedir. C-H bağlarının elektronegatiflik farkı az ve molekülde simetrik yapı olduğu için apolardır.
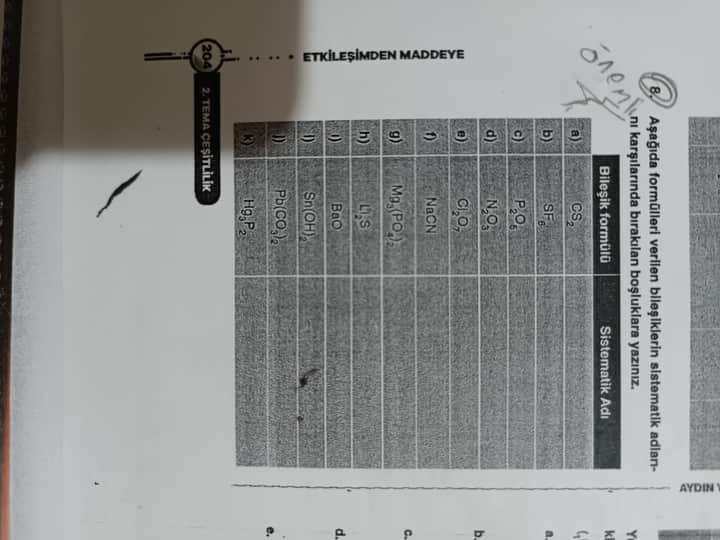
Soru: Aşağıda formülleri verilen bileşiklerin sistematik adlarını (IUPAC adı) yazınız.
Cevap:
Aşağıdaki tabloda, sıkça rastlanan bazı inorganik bileşiklerin yaygın formülleri ve IUPAC sistemine göre sistematik adları listelenmiştir. (Not: Sorulardaki tam formüller tabloda gösterilene yakın veya aynı olabilir; tablo geneldir.)
| Bileşik Formülü | Sistematik (IUPAC) Adı |
|---|---|
| Hg₂Cl₂ | Cıva(I) klorür (Mercury(I) chloride) |
| PbCO₃ | Kurşun(II) karbonat (Lead(II) carbonate) |
| Sn(OH)₂ | Kalay(II) hidroksit (Tin(II) hydroxide) |
| BaO | Baryum oksit (Barium oxide) |
| Li₂S | Lityum sülfür (Lithium sulfide) |
| Mg₃(PO₄)₂ | Magnezyum fosfat (Magnesium phosphate) |
| NaCN | Sodyum siyanür (Sodium cyanide) |
| N₂O | Dinitrojen monoksit (Nitrous oxide) |
| P₂O₅ | Difosfor pentoksit (Diphosphorus pentoxide) |
| NO₂ | Azot dioksit (Nitrogen dioxide) |
| P₂S₅ | Difosfor pentasülfür (Diphosphorus pentasulfide) |
| CS₂ | Karbon disülfür (Carbon disulfide) |
Önemli Açıklamalar:
- Stok (Stock) Nomenklatürü: Geçiş metalleri veya değişik değerlikli metaller için metalin değerlik numarası Romen rakamıyla belirtilir (örneğin, Pb(II) → Kurşun(II)).
- Yaygın Adlar: Bazı bileşiklerin eski adları da kullanılabilir (örneğin, Hg₂Cl₂ için “Kalomel”). Ancak sistematik kimyada stok ismi tercih edilir.
- Molekül Formülü: Soruda tam formül belirtilmemişse, burada listelenenler tipik örnekler olarak verilmiştir. Aynı mantıkla diğer benzer bileşikler de adlandırılabilir.
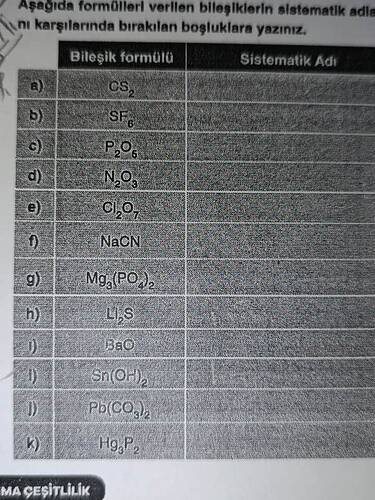
Soru: Aşağıda formülleri verilen bileşiklerin sistematik (IUPAC) adlarını yazınız.
Cevap:
Aşağıdaki tabloda her bir bileşiğin sistematik adı (Türkçe stok adı ve/veya IUPAC karşılığı) verilmiştir:
| Bileşik Formülü | Sistematik (IUPAC) Adı |
|---|---|
| CS₂ | Karbon disülfür |
| SF₆ | Kükürt hekzaflorür |
| P₂O₅ | Difosfor pentoksit (IUPAC’ta “pentaoksit”) |
| N₂O₃ | Dinitrojen trioksit |
| Cl₂O₇ | Diklor heptaoksit |
| NaCN | Sodyum siyanür |
| Mg₃(PO₄)₂ | Magnezyum fosfat |
| Li₂S | Lityum sülfür |
| BaO | Baryum oksit |
| Sn(OH)₂ | Kalay(II) hidroksit |
| Pb(CO₃)₂ | Kurşun(IV) karbonat |
| Hg₃P₂ | Cıva(II) fosfür |
Kısa Bilgiler ve İpuçları
- Ametaller arası bileşiklerde önce gelen ametalin sayısı (mono, di, tri…), ardından ikinci ametal için (mono, di, tri…) kullanılır. Örneğin, CO₂: Karbon dioksit, N₂O₃: Dinitrojen trioksit vb.
- Metal–ametal bileşiklerinde metalin yükseltgenme basamağı Romen rakamıyla (Stok sistemine göre) belirtilir. Örneğin, Sn(OH)₂ için “Kalay(II) hidroksit.”
- “(CO₃)” grubunun yükü -2 olduğundan Pb(CO₃)₂ bileşiğinde Kurşun toplam +4 değerlik alır: “Kurşun(IV) karbonat.”
Soru: Yukarıda top-çubuk formülleri verilen CO₂, CH₂O, NH₃ ve O₂ moleküllerinin polarlığını belirleyiniz ve yoğun fazlardaki (sıvı/katı hâl) moleküller arası etkileşim türlerini yazınız.
Cevap:
Aşağıdaki tabloda her molekülün polarlığı ve yoğun fazdaki başlıca moleküller arası etkileşim türleri özetlenmiştir:
| Molekül | Polarlık | Yoğun Fazdaki Başlıca Etkileşim Türü |
|---|---|---|
| CO₂ | Apolar (nonpolar) | London Dağılım Kuvvetleri (Geçici dipol-dipol) |
| CH₂O | Polar | Dipol-dipol etkileşimleri ve London Dağılım Kuvvetleri |
| NH₃ | Polar | Hidrojen Bağı + Dipol-dipol + London Dağılım Kuvvetleri |
| O₂ | Apolar (nonpolar) | London Dağılım Kuvvetleri (Geçici dipol-dipol) |
Önemli Noktalar
- CO₂ (Karbon dioksit) lineer yapısından dolayı net dipol momenti sıfırdır ve apolardır.
- CH₂O (Formaldehit) molekülü, kutuplu (polar) C=O grubu içerir; geometrisi üçgen düzlemli sayılabilir, net dipol momenti vardır.
- NH₃ (Amonyak) molekülü, üçgen piramidal geometriye sahip olup N–H bağı nedeniyle hidrojen bağı kurabilir ve oldukça polardır.
- O₂ (Oksijen) molekülü iki atomlu ve apolardır. Elektronlar eşit paylaşıldığından net dipol momenti sıfırdır.
Not: Hidrojen bağı, F–H, O–H veya N–H gibi son derece kutuplu bağların bulunduğu ve komşu molekül üzerinde uygun lone pair (yalnız çift) bulunan durumlarda ortaya çıkar. Bu nedenle NH₃ yoğun fazda hidrojen bağı kurabilmektedir.
Soru: Yukarıdaki tabloda verilen H₂, H₂S, He, NaBr, KCl, I₂, HCl, CO₂ ve H₂O maddelerinin yoğun fazdaki etkileşim türleriyle ilgili şu soruları cevaplayınız:
a) Hangileri sadece London (dağılım) kuvvetleriyle bir arada tutulur?
b) Hangilerinde kalıcı (permanent) dipol bulunur?
c) Hangileri arasında dipol-dipol etkileşimi kurulabilir?
d) Hangileri apolar moleküllerdir?
e) Hangileri iyonik bağlı bileşiklerdir?
Cevap:
Aşağıdaki tabloda her maddenin kısaca polarlığı ve yoğun fazdaki baskın etkileşimi özetlenmiştir:
| Madde | Polarlık / Yapı | Yoğun Fazdaki Başlıca Etkileşim |
|---|---|---|
| H₂ | Apolar (Homonükleer diatomik) | Yalnızca London (Dağılım) Kuvvetleri |
| H₂S | Polar (Açısal molekül) | Dipol-dipol ve London (Dağılım) Kuvvetleri |
| He | Tek atomlu, Apolar | Yalnızca London (Dağılım) Kuvvetleri |
| NaBr | İyonik (Metal + Ametal) | İyonik Bağlar |
| KCl | İyonik (Metal + Ametal) | İyonik Bağlar |
| I₂ | Apolar (İki atomlu, aynı element) | Yalnızca London (Dağılım) Kuvvetleri |
| HCl | Polar (Diatomik, farklı atomlar) | Dipol-dipol ve London (Dağılım) Kuvvetleri |
| CO₂ | Apolar (Lineer molekül) | Yalnızca London (Dağılım) Kuvvetleri |
| H₂O | Polar (Açısal molekül, H-bağı) | Hidrojen Bağı + Dipol-dipol + London (Dağılım) Kuvvetleri |
a) Sadece London (Dağılım) Kuvvetleri
H₂, He, I₂, CO₂
b) Kalıcı Dipol Bulunduranlar
H₂S, HCl, H₂O
(Not: Kalıcı dipol = polar molekül)
c) Dipol-Dipol Etkileşimi Kurulabilenler
Polar moleküller olduğu için H₂S, HCl, H₂O (H₂O ayrıca hidrojen bağı da kurar)
d) Apolar Moleküller
H₂, He, I₂, CO₂
e) İyonik Bağlı Bileşikler
NaBr, KCl
dokuzuncu hariciye koĝuşu hikayesinin incilenmesi
Dokuzuncu Hariciye Koğuşu Hikâyesinin İncelenmesi
Dokuzuncu Hariciye Koğuşu, Peyami Safa’nın modern Türk edebiyatındaki önemli eserlerinden biridir. 1930 yılında yayımlanan bu roman, yazarın hem biyografik detaylarını hem de toplumsal meselelerini ustalıkla harmanladığı bir metin olarak dikkat çeker. Aşağıda eserin detaylı incelemesi bulunmaktadır.
1. Konu
Eser, genç bir delikanlının bacak kemiğindeki rahatsızlığı yüzünden uzun yıllar hastalıkla mücadelesini, hastane ortamını ve bu süreçte yaşadığı psikolojik, sosyal ve duygusal sıkıntıları anlatır. Romanın ana odak noktası, kahramanın hastalıkla mücadele ederken yaşamını sorgulaması ve hayata tutunma çabasıdır.
2. Tema
Romanın ana teması, acı ve mücadele üzerinedir. Zengin olarak ele alınan diğer temalar şunlardır:
- Hastalık ve Hayat Mücadelesi: Fiziksel rahatsızlık, bireyin yaşamını ne denli değiştirdiğini göstermektedir.
- Yalnızlık: Hastalıkla mücadele sırasında hissedilen yalnızlık ve dış dünya ile kopukluk.
- Psikolojik Gerilim: Kahramanın iç dünyasında yaşadığı korkuları, kaygıları ve ölüm düşüncesi.
- Toplumsal Eleştiri: Dönemin toplumsal yapısına, özellikle doktor-hasta ilişkisine bakış.
3. Mekan
Roman, isminden de anlaşılacağı üzere hastane koğuşunda geçmektedir. Hastane atmosferi, insanın fiziksel ve psikolojik sıkıntılarının yoğunlaştığı küçük bir dünya olarak tasvir edilir. Ayrıca, kahramanın ev ortamı ve hastane dışındaki kısa sosyal ortamlar da anlatılır.
Mekânın Özellikleri:
- Hastane, soğuk ve steril bir mekan olarak tasvir edilir ve kahramanın yalnızlık hissini derinleştirir.
- Ev ile hastane arasındaki zıtlık, hastanın psikolojik durumunu net bir şekilde ortaya koyar.
4. Karakterler
| Karakter | Özellikleri |
|---|---|
| Genç Adam (Anlatıcı) | Romanın ana kahramanı, sürekli hastalıkla mücadele eden bir gençtir. Derin bir iç sorgulama yaşar. |
| Doktorlar | Hastalarını genellikle mesafeli ve profesyonel bir şekilde ele alırlar. Ancak bazen anlayışlı tavırlar da görülür. |
| Anne | Şefkatli, ancak çaresiz bir figürdür. Çocuğunu iyileştirme çabasıyla derin bir hüzün taşır. |
| Nüzhet | Kahramanın duygusal yakınlık kurduğu genç kızdır. Hem tutku hem hayal kırıklıklarıyla ilişkileri karmaşıktır. |
5. Üslup
Peyami Safa, roman boyunca oldukça içe dönük ve psikolojik bir üslup kullanır. Anlatıcının zihinsel süreçleri, duygusal gelgitleri uzun iç monologlarla okuyucuya aktarılır. Üslup özellikleri:
- Tasvir ve Betimleme: Mekân, karakterlerin ruh halleri ve çevre detaylarını tasvir etmede başarılıdır.
- Duygusal Yoğunluk: Genç adamın yaşadığı duyguların anlatımı sık sık abartılı veya yoğun bir biçimde verilir.
- Gerçekçi Yaklaşım: Hastane, hastalık, tedavi süreçleri doğal ve gerçekçi bir şekilde aktarılır.
6. Edebi Tür ve Anlatım Tekniği
- Tür: Roman.
- Anlatım Tekniği: Birinci tekil şahıs anlatımı benimsenmiştir. Genç adamın gözünden hayatı ve duygusal durumları öğreniriz.
- İç konuşma tekniği: Karakterin zihinsel gerilimleri, bu teknik ile okuyucuya aktarılır.
- Olay örgüsü: Kronolojik olarak ilerleyen fakat kahramanın iç dünyasındaki karmaşa ile paralel bir şekilde derinleşen bir yapıdadır.
7. Romanın Ana Fikri
Hayat, mücadeleler ve acılarla doludur; insan, bu zorluklara rağmen yaşamamı anlamlandırabilir. Umutsuzluklar içinde bile tutunacak bir umut ışığı vardır.
8. Peyami Safa ve Eserin Biyografik Yönü
Peyami Safa’nın kendisi de çocukluk yıllarında uzun süre kemik hastalığıyla mücadele etmiştir. Bu açıdan roman, yazarın kendi yaşamından izler taşır. Bireysel acılarının edebiyat aracılığıyla dışa vurumu olarak görülebilir.
9. Romanın Değerlendirilmesi
- Edebi Değer: Türk edebiyatında psikolojik roman türünde önemli bir yere sahiptir. Peyami Safa’nın derin gözlem yeteneği ve içsel analiz gücü bu eserde belirgin bir şekilde görülür.
- Toplumsal Mesaj: Romandaki hastalık, yalnızlık ve mücadele unsurları, geniş bir okuyucu kitlesinin duygusal bağ kurabileceği evrensel temalardır.
- Dil ve Üslup: Akıcı, yer yer dokunaklı bir üsluba sahiptir.
10. Özet
| Bölüm | Olay |
|---|---|
| Hastalık Süreci | Genç adam bacak kemiğindeki rahatsızlık nedeniyle sürekli hastane tedavisi görmektedir. |
| Psikolojik Sıkıntılar | Ölüm korkusu, hayatta anlam bulma çabası, yalnızlık duygusu derinlemesine işlenir. |
| Anne ve Doktorlar | Anne sevgisi ve doktorların profesyonelliği arasındaki mücadele, hastane ilişkileri ekseninde anlatılır. |
| Nüzhet ile İlişki | Genç adamın hastalık sürecinde duygusal yakınlık geliştirdiği Nüzhet ile olan karmaşık ilişkisi. |
Sonuç
Dokuzuncu Hariciye Koğuşu, bireysel mücadeleleri ve insan ruhunun karmaşıklığını ele alan çok yönlü bir roman olarak Türk edebiyatındaki yerini almıştır. Peyami Safa’nın önerdiği yaşam mücadelesi fikri, okuyuculara derin bir düşünme fırsatı sunar.
Tablo: Romanın Önemli Unsurlarının Özeti
| Kategori | Detay |
|---|---|
| Tema | Acı, mücadele, yalnızlık, psikolojik gerilim |
| Karakterler | Genç adam, doktorlar, Nüzhet, anne |
| Mekân | Hastane koğuşu, hasta ev ortamı |
| Anlatım Tekniği | İç konuşma, olay örgüsü |