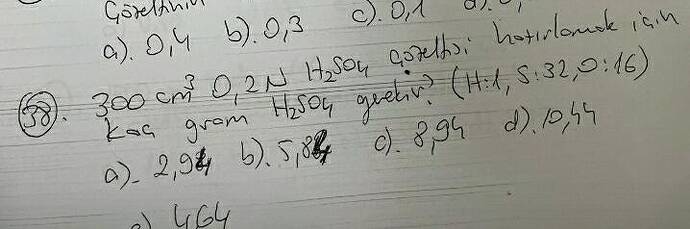Çözümü:
Verilen Bilgiler:
- Çözeltinin hacmi: (300 , \text{cm}^3) (yani (0.3 , \text{L}))
- Çözeltinin normalitesi (N): (0.2 , \text{N})
- H(_2)SO(_4)'ün moleküler ağırlığı: (2 \times 1 + 32 + 4 \times 16 = 98 , \text{g/mol})
Çözüm Aşamaları:
-
Normalite (N) Tanımı: Normalite, 1 litre çözeltideki ekvivalent ağırlıkla ilgili bir konsantrasyon birimidir. H(_2)SO(_4) için 1 mol asit, 2 ekvivalent asit verir çünkü H(_2)SO(_4) iki proton (H(^+)) verebilir. Bu yüzden, H(_2)SO(_4)'ün ekvivalent ağırlığı, moleküler ağırlığın proton sayısına bölünmesiyle hesaplanır:
\frac{98 \, \text{g/mol}}{2} = 49 \, \text{g/ekv} -
Gerekli Ekvivalent H(_2)SO(_4) Miktarını Hesaplama:
Normalite formülü:
\text{Normalite} = \frac{\text{Ekvivalent gram sayısı}}{\text{Hacim (L)}}Buradan, ekvivalent gram sayısını hesaplayabiliriz:
0.2 = \frac{\text{Ekvivalent gram sayısı}}{0.3}Ekvivalent gram sayısı:
\text{Ekvivalent gram sayısı} = 0.2 \times 0.3 = 0.06 \, \text{ekv} -
Ağırlığın Hesaplanması:
Ekvivalent gram sayısı, H(_2)SO(_4)'ün ağırlığına dönüştürülür:
\text{Gram cinsinden ağırlık} = \text{Ekvivalent gram sayısı} \times \text{Ekvivalent ağırlık}\text{Gram cinsinden ağırlık} = 0.06 \times 49 = 2.94 \, \text{g}
Final Cevap:
300 cm(^3) 0.2 N H(_2)SO(_4) çözeltisi hazırlamak için 2.94 gram H(_2)SO(_4) gerekir. Bu, seçenekler arasında yer almadığından sorunun cevabı yanlış verilmiş olabilir. Konu daha fazla netleştirilebilir.