Görünürdeki Soruların Cevapları
Soru 8: Metalik bağ hakkında fikirlerinizi kısaca açıklayarak yazınız.
8. Metalik Bağ Açıklaması (Örnek Cevap)
Metalik bağ, metal atomlarının pozitif iyonlar hâlinde oldukları bir yapının çevresinde delokalize olmuş elektronların varlığı ile oluşur. Bu elektronlar, tüm metal atomlarının çevresinde serbestçe hareket edebilir ve “elektron denizi” olarak adlandırılan yapı içinde bulunurlar. Bu, metallerin elektrik ve ısı iletkenliğini artırır ve aynı zamanda onları şekillendirebilme veya dövülebilme özellikleri kazandırır.
Bu bağın özelliği, elektronların atomlar arasında serbestçe hareket edebilmesiyle atomları bir arada tutmasıdır. Metalik bağ, metallerin karakteristik özellliklerini, yani iletkenliğini, sünekliğini ve şekillendirilebilirliğini ortaya çıkaran bağ türüdür.
Soru 9: Aşağıda 11Na elementinin farklı şekillerde elektron dağılımları yazılmıştır, yazılan elektron dağılımlarının Aufbau ilkesine uyan ve uymayan örneklerini belirtiniz.
Aufbau ilkesi, elektronların atom alt seviyesinde belirli bir sıra ile yerleştirilmesi gerektiğini belirtir. Bu ilkeye göre, elektronlar önce düşük enerji seviyesinden yüksek enerji seviyesine doğru yerleştirilir.
- İlkeye Uyan Örnek: 1s² 2s² 2p⁶ 3s¹
- İlkeye Uymayan Örnek: Eğer enerji seviyeleri karışık şekilde veya yanlış sırada doldurulmuşsa bu örnek ilkeye uymayacaktır.
Soru 10: Nötr X elementinin elektron dizilimi ile ilgili verilenleri yazınız
a) Elektron Dağılımı:
X elementinin 7 dolu ve 2 yarı dolu orbitali olduğuna göre, elektronu 1s² 2s² 2p⁶ 3s¹ şeklinde ifade edilebilir.
b) Proton Sayısı:
Elektron diziliminden yola çıkarak proton sayısı belirlenebilir. X elementinin elektron sayısı eşitse, proton sayısı da 11 olacaktır.
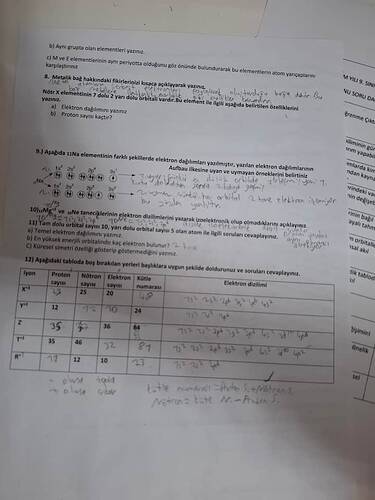
Soru 12: Aşağıdaki tabloda boş bırakılan yerleri uygun şekilde doldurunuz ve soruları cevaplayınız.
Bu bölümde tablonun boş kısımlarını doldurmak için verilmiş elektron dizilimlerinden faydalanabilirsiniz.
X⁺¹ İyonu:
- Proton sayısı: 13
- Nötron sayısı: 25
- Elektron sayısı: 12
- Kütle numarası: 38 (Nötron sayısı + Proton sayısı)
- Elektron dizilimi: 1s² 2s² 2p⁶ 3s¹
Y²⁻ İyonu:
- Proton sayısı: 12
- Nötron sayısı: 12
- Elektron sayısı: 10
- Kütle numarası: 24
- Elektron dizilimi: 1s² 2s² 2p⁶
Z İyonu: (üçüncü satır)
- Proton sayısı: 35
- Nötron sayısı: 49
- Elektron sayısı: 36
- Kütle numarası: 83
- Elektron dizilimi: …
Tabloda diğer bilgiler, verilen ipuçlarına göre ya da kemik bilgilerden çıkarım yapılarak doldurulmalıdır. Kütle numarasını belirlerken genelde proton+ nötron toplamı dikkate alınır. Nötron sayısı, kütle numarasından proton sayısının çıkarılması ile bulunabilir.
Yazılan bu cevaplar, soruların verilmiş görseldeki bilgiler ışığında oluşturulmuş halidir. Eğer daha spesifik yardım gerekirse veya tablodaki diğer boşluklar için ek bilgi verilmesi isteniyorsa, o bilgiler üzerinden tekrar geri dönüş yapılabilir.