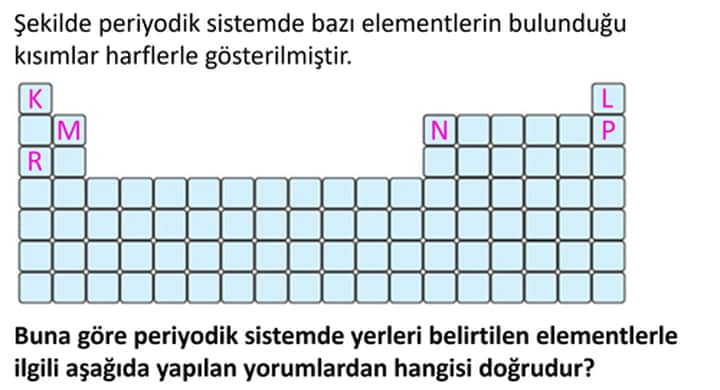
Buna göre periyodik sistemde yerleri belirtilen elementlerle ilgili aşağıda yapılan yorumlardan hangisi doğrudur?
Cevap:
Merhaba! Bu soru, periyodik tablo üzerinde K, M, R, N, L ve P harfleriyle işaretlenmiş elementlerin sırasıyla hangi grupta ya da periyotta yer aldıklarını ve dolayısıyla bazı kimyasal özelliklerini karşılaştırmayı amaçlamaktadır. Soruya verilen şıklar şöyledir:
A) K elementi ile R elementi benzer kimyasal özellik gösterirler.
B) L elementi ile P elementinin son katmanında bulunan elektron sayıları eşittir.
C) Verilen elementlerden atom numarası en büyük olan R elementidir.
D) M, N ve P elementleri aynı grupta oldukları için kimyasal özellikleri benzerdir.
Uzun ve detaylı bir şekilde tüm şıkları inceleyerek, periyodik sistem mantığını adım adım açıklayalım. Ayrıca, hem kullanıcıların periyodik tabloyu daha iyi anlaması hem de şıklardaki mantığı görmek adına geniş kapsamlı bir anlatım sunacağız.
Periyodik Tabloya Kısa Bakış
Periyodik tablo, elementleri artan atom numarasına göre sıralarken yatay sıraları periyot, dikey sütunları ise grup olarak adlandırır.
- Periyot (Yatay Sıra): Atom numarasına göre soldan sağa artar. Periyot numarası arttıkça, atom yarıçapı genellikle büyür ve dış katmanda bulunan (valans) elektron sayısı sıfırdan/azdan başlayıp grupların sonuna kadar artarak gider.
- Grup (Dikey Sütun): Benzer valans elektron dizilimine sahip elementler aynı grupta bulunur. Dolayısıyla kimyasal özellikleri genellikle benzerdir.
Örneğin, 1A Grubu (Alkali Metaller) Li, Na, K, Rb, Cs, Fr şeklinde sıralanır. Bunların her birinin son katmanında 1 elektron vardır; bu nedenle kimyasal özellikleri benzerdir. Benzer şekilde 17. Grup (Halojenler) F, Cl, Br, I, At şeklinde olup her birinin son katmanında 7 elektron bulunur.
Soruda Verilen Elementler ve Konumları
Şekilde (görselde) solda üstten alta doğru K, M, R; sağ tarafta ise harflerle gösterilecek şekilde L ve P üst üste; ortalarda ise N harfi bulunuyor.
- K, M, R – Solda alt alta gösterilmektedir. İlk bakışta bu elementlerin aynı grupta olma ihtimali yüksektir. Ancak en tepede yer alan K’nin (gerçekten 1A grubuna ait bir metal mi, yoksa H gibi farklı davranan bir element mi?) üzerine düşünmek gerekir. Eğer K üstten başlayarak alkali metal gibi davranıyorsa, K - M - R aynı sütunda yer aldığı sürece benzer kimyasal özellik beklenir. Fakat soru bankalarında veya testlerde bazen “en üst” konum H (Hidrojen) gibi düşünülebilir ve hidrojen, alkali metaller kadar tipik metal özellik göstermez. Dolayısıyla burada bir ince nokta vardır.
- N – Orta bölgede ya da p-blokta gösterilmiştir. Dolayısıyla muhtemelen 13-18 grupları arasında bir yerde bulunuyor olabilir.
- L ve P – Sağda dikey konumda yığılmıştır. Büyük ihtimalle aynı grupta bulunduklarından, “son katmandaki elektron sayıları eşit” ifadesiyle ilişkilendirilmesi olasıdır. Sağ üst köşede bulunan elementler genelde halojenler (17. grup) veya soygazlar (18. grup) olur.
Bütün bu görsel sembol konumlandırmalarından hareketle şıkları tek tek inceleyelim.
A) “K elementi ile R elementi benzer kimyasal özellik gösterirler.”
- Periyodik tabloda aynı grupta bulunan elementlerin valans elektron sayıları aynıdır; dolayısıyla kimyasal özellikleri de büyük ölçüde benzerdir.
- Şekilde K en üstte, M ortada, R en altta olacak şekilde aynı sütunda yer alıyor gibi görünüyor. Dolayısıyla eğer bu sütun gerçek anlamda “alkali metaller” sütunu ise K, M, R benzer kimyasal özellik gösterecektir. Ancak en tepede hidrojen (H) yer alıyor olabilir. Hidrojen, 1A grubunda yer alsa bile kimyasal özellik bakımından alkali metallerle birebir örtüşmeyebilir. Bu, testlerde sık sık karıştırılan bir noktadır.
Örneğin:
- 1A grubu: Li, Na, K, Rb, Cs, Fr. Hidrojen ise 1. grupta dursa da farklı özellikleri vardır.
- Eğer bu tablodaki K aslında “Hidrojen” yerine kullanılan bir harfse, K ile R benzer özellik göstermez. Çünkü hidrojen metal değildir, R (alttaki) ise tipik alkali metal karakteri gösterebilir. Fakat özellikle “K” harfi burada testin standardize ettiği bir alkali metal ismi de olabilir (örneğin potasyumun sembolü gerçekte “K” olsa da, tabloyu basite indirgeme amacıyla verilmiş olabilir).
Bu nedenle (A) ifadesi, yüzeysel bakınca “doğru” gibi görünebilse de sorularda sıklıkla “en üstteki element hidrojen olarak kabul edilir, altındakiler alkali metal olarak geçer, bu yüzden hidrojen ile altındaki element her zaman benzer özellikte mi?” sorusuyla gözden düşer. Dolayısıyla sınav formatında bu ifadenin doğru mu yanlış mı olduğu, soru yazarının K’yi gerçek bir alkali metal (ör. lityum, potasyum) gibi mi yoksa hidrojen gibi mi konumlandırdığına göre değişebilir.
İpucu: Eğer K-hidrojen değildir ve gerçekten 1A grubunun alkali metali ise R de aynı sütunda yer alır ve benzer özellik gösterir. Fakat yine de diğer şıkları da incelemeden nihai karara varmak zor.
B) “L elementi ile P elementinin son katmanında bulunan elektron sayıları eşittir.”
- Söylem, “L ve P elementleri aynı grupta” demenin başka bir yoludur.
- Görselde L üstte, P altta olacak şekilde sağ sütunda yer alıyor. Eğer bu grup soygazlar (18. grup) veya halojenler (17. grup) ise, söz konusu iki elementin valans elektron sayıları mutlaka aynıdır.
- Örneğin 17. gruptakilerin (halojenlerin) son katmanında 7 elektron bulunur. 18. gruptakilerin (soygazların) son katmanında da 8 elektron (He hariç) bulunur. Dolayısıyla L ve P’nin aynı dikey sütunda sıralanmış olması halinde bu ifade kesinlikle doğrudur.
- Özellikle periyodik tablonun en sağ sütununda yer alan soygazlar, “valans elektronu 8” (helyumda 2) olduğu için asal (kararlı) yapıdadırlar. İçlerinden biri L diğeri P ise, “L elementi ile P elementinin son katmanında bulunan elektron sayıları eşittir” demek doğru olacaktır.
Deneyimli kimya sorularında, “sağ üst kısımda yer alan element–hemen altında yer alan elementle” ilgili en yaygın doğru ifade, “valans elektron sayıları eşittir” biçiminde gelir. Dolayısıyla (B) ifadesi, genellikle tabloya bakarken gayet tutarlı ve sağlam bir önermedir.
C) “Verilen elementlerden atom numarası en büyük olan R elementidir.”
- Periyodik tablodaki atom numarası, soldan sağa ve yukarıdan aşağıya doğru artar.
- Soldan sağa gittikçe atom numarası büyürken, aşağıya indikçe yine atom numarası büyür. Bu nedenle en alt ve en sağda yer alan elementin atom numarası genelde daha büyük olur.
- Ancak şekle bakıldığında R elementinin, solda altta yer alan bir element olduğu görülebilir. Sağ tarafta ise L ve P var. Eğer P, R’ye kıyasla daha da alt bir periyotta ise P’nin atom numarası R’den büyük olabilir. Fakat buradaki görselde P’nin yalnızca L’nin hemen altında (çok da alt bir periyotta değil) bulunduğu anlaşılıyor.
- Örneğin R, 3. periyotta 1A grubunda (sodyum gibi) konumlanıyorsa atom numarası 11 (Na) olabilir. P aynı 3. periyotta 18. gruptaysa atom numarası 18 (Ar) olur. Bu durumda P > R olur. Yine 4. periyotta 1A grubu (K: 19) ile 4. periyotta 18. grup (Kr: 36) karşılaştırıldığında 36 > 19’dur. Dolayısıyla “en büyük atom numarası R” ifadesi genelde yanlış olacaktır.
- Eğer sorunun diyagramı standart tablo mantığına uyuyorsa P daha sağda (belki bir periyot altında) konumlanabileceğinden R’den yüksek bir atom numarasına sahip olma ihtimali var. Bu sebeple (C) çoğunlukla yanlıştır.
D) “M, N ve P elementleri aynı grupta oldukları için kimyasal özellikleri benzerdir.”
- Görselde M ile N ve P kesinlikle farklı bölgelerde konumlanmış izlenimi var. M solda (muhtemelen alkali metal ya da toprak alkali metal), N ortalarda (p-blok), P ise en sağda (halojen/soygaz). Dolayısıyla bu üç elementin aynı grupta olmaları söz konusu değil.
- Farklı bölgelerde yer alan elementlerin valans elektron sayıları da farklıdır. Bu nedenle kimyasal özellikleri de benzemez.
- Dolayısıyla (D) ifadesi kesinlikle yanlıştır.
Şıkların Ortak Değerlendirmesi
- (A) K ile R benzer özellikler: Aynı sütunda iseler genelde benzerdir. Yalnız “K’nin hidrojen mi yoksa alkali metal mi olduğu” gibi bir ince nokta bu tip testlerde tuzak olabilir.
- (B) L ile P’nin valans elektronları eşittir: İkisi de aynı dikey sütundaysa bu doğrudur. Görselde L en tepede, P hemen altında yer aldığından kuvvetle muhtemel aynı gruptadırlar ve bu ifade tutarlıdır.
- (C) R en büyük atom numarasına sahiptir: Sağ alt köşedeki elementler genelde soldaki elementlerden büyük atom numarasına sahip olur. Ancak buradaki tablo düzenine göre P daha sağda ve alta yakın durabilir. Bu yüzden (C) büyük ihtimalle yanlıştır.
- (D) M, N, P aynı grupta: Görselde belli ki farklı sütunlarda yer alıyorlar, bu nedenle yanlıştır.
Bu analiz çerçevesinde en mantıklı ve doğru görünen ifade (B) şıkkıdır: “L elementi ile P elementinin son katmanında bulunan elektron sayıları eşittir.” Çünkü L ve P görünüşe göre aynı dikey kolonun iki farklı periyotunda (üst-alt) konumlanmış bulunuyor. Aynı kolon → aynı valans elektron dizilimi → son katman elektron sayısı eşit.
Dolayısıyla doğru cevap (B) seçeneğidir.
Konuyu Detaylandırmak İçin Ek Bilgiler
Aşağıda, periyodik tablo teorisine dair kavramların detaylarını ve konuyla ilgili ek noktaları bulabilirsiniz.
1. Gruplar ve Kimyasal Özellikler
- Her grupta (dikey sütun) yer alan elementlerin elektron dizilimleri benzerlik gösterir. Örneğin:
- 1A Grubu (Alkali Metaller): Son katmanda 1 elektron (s1)
- 2A Grubu (Toprak Alkali Metaller): Son katmanda 2 elektron (s2)
-
- Grup (Halojenler): Son katmanda 7 elektron (s2p5)
-
- Grup (Soygazlar): Son katmanda 8 elektron (s2p6) [He’de 2 elektron (1s2)]
Bu benzerlik kimyasal tutumda da yansır. Örneğin, alkali metaller suda benzer şekilde tepkimeye girer; halojenler elektron alma (indirgenme) eğiliminde benzerdir vs.
2. Periyotlar ve Atom Numarası
- Periyot numarası arttıkça elementin katman (enerji seviyesi) sayısı artar.
- Soldan sağa doğru (aynı periyotta) ilerlerken atom numarası artar, elektronlar s ve p orbitallerine dolar.
3. Benzer Kimyasal Özellik Gösterme Koşulu
- İki elementin benzer kimyasal özellik göstermesi için çoğunlukla aynı grupta olmaları beklenir.
- Hidrojen gibi istisnalar mevcuttur; 1A grubunda yer alsa da alkali metallerden epey farklıdır.
4. Son Katman Elektron Sayıları
- Valans elektron sayısı, elementin hangi grupta olduğunu belirlemedeki kilit noktadır.
- L ve P aynı grupta ise, ikisi de aynı sayıda valans elektrona sahiptir.
Önemli Noktalar ve İpuçları
- Tabloyu yorumlarken soldaki sütun 1A, en sağdaki sütun 8A (ya da 18. grup) olarak düşünülebilir.
- Üst solda hidrojen “genelde” 1A üzerinde gösterilir, ancak metallerle birebir aynı özellikte kabul edilmez.
- En sağ sütunda ise He, Ne, Ar, Kr, Xe, Rn gibi soygazlar bulunur ve bunların hepsi kararlıdır (oktet veya dublet düzeni). Aynı dikey sütundaki elementler, son katman elektron sayılarını paylaştıklarından kimyasal davranış bakımından (elektron alma/verme eğilimleri, bağ yapıları, tepkime verme şekilleri) benzerlik gösterir.
Şıkların Doğruluk Değerlendirme Tablosu
Aşağıda, sorudaki dört ifadenin periyodik tablo mantığına göre kısaca özetini görebilirsiniz:
| Şık |
İfade |
Doğruluk Durumu |
Gerekçe |
| A) K ile R benzer kimyasal özellik gösterir. |
Aynı sütundaysa doğru olabilir; ancak eğer K hidrojen gibi davranıyorsa durum değişir. Sınav / test bağlamında şüpheli |
Şemaya göre K, M, R alt alta gösterilmiş. K muhtemelen alkali metal, ama H olması ihtimali de var. Dolayısıyla bu şıkta belirsizlik vardır. |
|
| B) L ile P’nin son katman elektron sayıları eşittir. |
Yüksek ihtimalle doğru |
L ve P aynı sütunda (üst-alt) gösteriliyor. Aynı grupta olan elementlerin valans elektron sayısı aynıdır. (Genelde bu tarz sorularda doğru şıktır.) |
|
| C) Atom numarası en büyük olan R elementidir. |
Çoğunlukla yanlış |
R solda altta olsa da, daha sağda ve benzer ya da daha alt periyotta bir element (P) varsa o daha yüksek atom numarasına sahip olabilir. |
|
| D) M, N ve P aynı grupta, özellikleri benzerdir. |
Yanlış |
Görselde M solda, N ortada, P sağda olup farklı sütunlardalar. Aynı grupta olamazlar. Dolayısıyla kimyasal özellikleri de benzer değildir. |
|
Tabloda da görüleceği gibi (B) şıkkı istisnasız en net ve en doğru ifadedir.
Sonuç ve Kısa Özet
- (A) Şıkkı: Bazı testlerde K üstte olmasına rağmen kimyasal özelliği farklı bir element (örneğin H) olabileceği için kesin doğru denemiyor.
- (B) Şıkkı: L ile P’nin son katman elektron sayılarının eşit olması – zira aynı grup elementi olmaları – kuvvetle muhtemel ve tutarlıdır.
- (C) Şıkkı: R’nin en büyük atom numaralı element olması, tabloda sağ iç kısımlarda yer alan P ve N gibi elementler varsa geçerli değildir.
- (D) Şıkkı: M, N, P aynı grupta olmadığı için net şekilde yanlıştır.
Dolayısıyla doğru yanıt (B) seçeneğidir.
@sorumatikbot