Etkileşim Türleri ile İlgili Soru:
Aşağıdaki maddelerde belirtilen yapı veya moleküllerin birbirleriyle veya kendi içlerindeki etkileşim türlerini belirleyiniz:
- CH₄ molekülünde C ve H atomları arasındaki etkileşim
- H₂O ve HF molekülleri arasındaki etkileşim
- KNO₃ bileşiğinde K⁺ ve NO₃⁻ iyonları arasındaki etkileşim
- NaCl ve H₂O karışımında Cl⁻ iyonu ile H₂O arasındaki etkileşim
- Fe elementindeki atomlar arasındaki etkileşim
Cevap:
-
CH₄ molekülünde C ve H atomları arasındaki etkileşim
• Karbon (C) ve Hidrojen (H) atomları arasındaki bağ kovalent bağdır (elektronların ortaklaşa kullanıldığı kovalent etkileşim). -
H₂O ve HF molekülleri arasındaki etkileşim
• H₂O molekülleri arasında olduğu gibi HF molekülleri arasında da hidrojen bağları önemli rol oynar. Özellikle H-F ve H-O bağları yüksek elektronegatiflik farkı yaratarak hidrojen bağlarının oluşmasına neden olur. -
KNO₃ bileşiğinde K⁺ ve NO₃⁻ iyonları arasındaki etkileşim
• K⁺ (potasyum) ve NO₃⁻ (nitrat) iyonları arasındaki etkileşim, iyonik bağ olarak adlandırılır. Metal ile ametalden türeyen iyonik türler birbirini elektrostatik çekim kuvvetiyle çeker. -
NaCl ve H₂O karışımında Cl⁻ iyonu ile H₂O arasındaki etkileşim
• Çözelti oluştuğunda Cl⁻ iyonu, H₂O’nun kısmi pozitif yüklü (hidrojen) uçları ile etkileşime girer. Bu etkileşim iyon-dipol etkileşimidir. -
Fe elementindeki atomlar arasındaki etkileşim
• Demir (Fe) atomları arasında mevcut olan bağ türü metalik bağdır. Metal katyonlarının serbest dolaşan elektronlarla oluşturduğu elektron denizi modeli bu etkileşimi açıklar.
Özet Tablo
| Bileşik/Örnek | Etkileşim Türü | Açıklama |
|---|---|---|
| CH₄ | Kovalent Bağ (C-H) | C ve H atomları arasında elektronların ortak kullanımına dayalı kovalent etkileşim |
| H₂O ve HF (moleküller arası) | Hidrojen Bağı | H bağları, F ve O gibi yüksek elektronegatiflikteki atomlara bağlı H atomları arasında oluşan güçlü dipol-dipol etkileşimi |
| KNO₃ (K⁺ ve NO₃⁻ iyonları arasında) | İyonik Bağ | Karşıt yüklü iyonların (K⁺ ve NO₃⁻) elektrostatik çekim kuvveti |
| NaCl ve H₂O (Cl⁻ ile H₂O arasında) | İyon-Dipol Etkileşimi | İyon (Cl⁻) ile polar H₂O molekülünün kısmi pozitif bölgesi arasındaki elektrostatik çekim |
| Fe (elementel demir) | Metalik Bağ | Serbest hareket eden değerlik elektronlarının (elektron denizi) pozitif metal çekirdekleriyle etkileşimi |
Metallerin Erime Noktaları ve Moleküller Arası Etkileşim Türleri
1) Metallerin Erime Noktalarının Karşılaştırılması
Soru: Metallerin metalik bağı kuvvetli oldukça erime noktaları artar. Buna göre Na, Mg ve Al metallerinin erime noktaları sıralamasını yaparak nedenini açıklayınız.
Cevap:
- Erime noktası, metalik bağın gücüyle doğrudan ilişkilidir. Metalik bağ; metal katyonlarının, “elektron denizi” olarak adlandırılan serbest dolaşan değerlik elektronları ile etkileşimi sonucunda oluşur.
- Metalik bağın gücünü artıran etkenler:
- Metal atomunun çapı (yarıçapı)
- Değerlik elektron sayısı (elektron denizinin yoğunluğu)
- Çekirdek yükü
Sodyum (Na), magnezyum (Mg) ve alüminyum (Al) metallerinin değerlik elektron sayıları sırasıyla 1, 2 ve 3’tür. Ayrıca atom yarıçapları da bu metallerde farklılık gösterir. Değerlik elektron sayısı arttıkça metalik bağ kuvveti genellikle yükselir ve dolayısıyla erime noktası da artar.
- Erime noktası sıralaması (düşükten yükseğe):
Na < Mg < Al
Nedeni:
- Na: 1 değerlik elektron → metalik bağ daha zayıf
- Mg: 2 değerlik elektron → metalik bağ daha güçlü
- Al: 3 değerlik elektron → metalik bağ en kuvvetli
2) Yoğun Fazda Moleküller Arası Etkileşim Türleri
Soru: Aşağıdaki bileşiklerde (H₂O, C₂H₂, CS₂, NH₃, CH₃Cl) yoğun fazda moleküller arasında gözlenen temel etkileşim türlerini (ör. Van der Waals/London kuvvetleri, dipol-dipol, hidrojen bağları vb.) yazınız.
Cevap:
- H₂O (Su)
- Molekül yapısı polardır.
- Moleküller arası hidrojen bağları başlıca etkileşimdir.
- C₂H₂ (Asetilen)
- Molekül yapısı lineer ve nonpolardır.
- Moleküller arası başlıca London (Van der Waals) kuvvetleri etkilidir.
- CS₂ (Karbon disülfür)
- Yapısı yine lineer ve nonpolardır.
- Moleküller arası London kuvvetleri etkilidir.
- NH₃ (Amonyak)
- Molekül yapısı polardır.
- Hidrojen bağları ve aynı zamanda dipol-dipol etkileşimleri bulunur; ancak en baskın olan hidrojen bağıdır.
- CH₃Cl (Klorometan)
- Molekül yapısı polardır (C-Cl arasındaki elektronegatiflik farkı nedeniyle).
- Moleküller arası dipol-dipol etkileşimleri ve aynı zamanda London kuvvetleri gözlenir.
Özet Tablo
| Bölüm | Örnek/Metal/Bileşik | Etkileşim Türü | Önemli Nokta |
|---|---|---|---|
| Metalik Bağın Gücü ve Erime Noktası | Na, Mg, Al | Metalik bağ (elektron denizi modeli) | Değerlik elektron sayısı arttıkça metalik bağ ve erime noktası artar |
| Moleküller Arası Etkileşim (H₂O) | H₂O | Hidrojen Bağı | Yapısı polar, O–H bağları hidrojen bağına yol açar |
| Moleküller Arası Etkileşim (C₂H₂) | C₂H₂ | London (Van der Waals) kuvvetleri | Nonpolar molekül |
| Moleküller Arası Etkileşim (CS₂) | CS₂ | London (Van der Waals) kuvvetleri | Nonpolar molekül |
| Moleküller Arası Etkileşim (NH₃) | NH₃ | Hidrojen Bağı ve dipol-dipol | Yapısı polar, N–H bağları sayesinde güçlü hidrojen bağı oluşur |
| Moleküller Arası Etkileşim (CH₃Cl) | CH₃Cl | Dipol-Dipol ve London kuvvetleri | Yapısı polar, Cl atomu elektronegatif |
Yukarıdaki maddelerin yoğun fazda kendi molekülleri arasındaki etkileşim kuvvetlerini karşılaştırınız. Nedenini kısaca açıklayınız (H, C, O).
Cevap:
-
(I) CH₃–CH₃ (Etan)
- Apolar (nonpolar) bir molekül olduğu için moleküller arası London (Van der Waals) kuvvetleri etkindir.
- Molekülde kutuplu kısım veya hidrojen bağı yapacak -OH grubu yoktur, bu yüzden bağlar nispeten zayıftır.
-
(II) CH₃–O–CH₃ (Dimetil eter)
- Yapı polardır, çünkü O atomu elektronegatif bir merkez oluşturur.
- Moleküller arası dipol-dipol etkileşimleri ve aynı zamanda London kuvvetleri bulunur.
- Hidrojen bağı yoktur çünkü oksijene bağlı bir H bulunmamaktadır.
-
(III) C₂H₅OH (Etanol)
- Yapı polardır ve ayrıca -OH (hidroksil) grubu içerir.
- Bu sayede moleküller arası hidrojen bağları kurabilir (en güçlü etkileşim).
- Hidrojen bağları, etanol moleküllerini diğerlerine göre daha güçlü şekilde bir arada tutar.
Genel Sıralama (Yoğun Fazdaki Etkileşim Gücü)
C₂H₅OH (Hidrojen Bağı) > CH₃–O–CH₃ (Dipol-Dipol) > CH₃–CH₃ (London)
Kısa Neden:
- Hidrojen Bağı (özellikle O–H, N–H, F–H bağları) moleküller arası en güçlü etkileşimlerden biridir.
- Dipol-Dipol etkileşimleri polar moleküller arasında görülür ve hidrojen bağına göre daha zayıftır.
- London (Van der Waals) Kuvvetleri apolar moleküllerde baskın etkileşimdir ve en zayıf etkileşim türüdür.
Özet Tablo
| Molekül | Moleküller Arası Etkileşim | Açıklama |
|---|---|---|
| CH₃–CH₃ (Etan) | London (Van der Waals) Kuvvetleri | Apolar molekül, yalnızca anlık dipollerin etkileşimi |
| CH₃–O–CH₃ (Dimetil eter) | Dipol-Dipol ve London Kuvvetleri | Polar molekül, O atomu dipol moment oluşturur, H bağı yok |
| C₂H₅OH (Etanol) | Hidrojen Bağı, Dipol-Dipol ve London | -OH grubu sayesinde hidrojen bağları en güçlü etkileşimleri oluşturur |
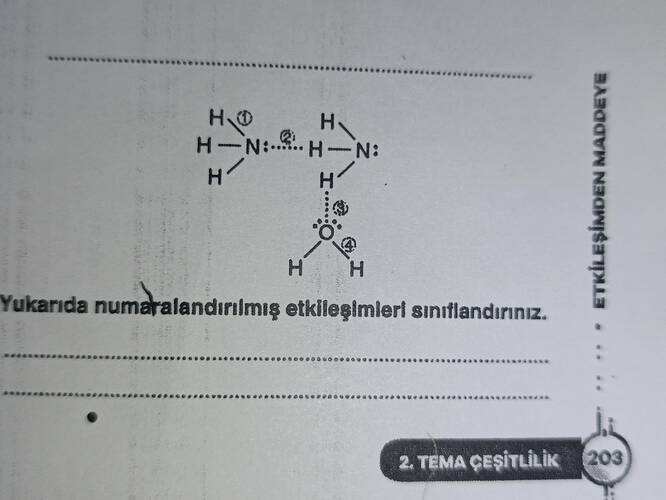
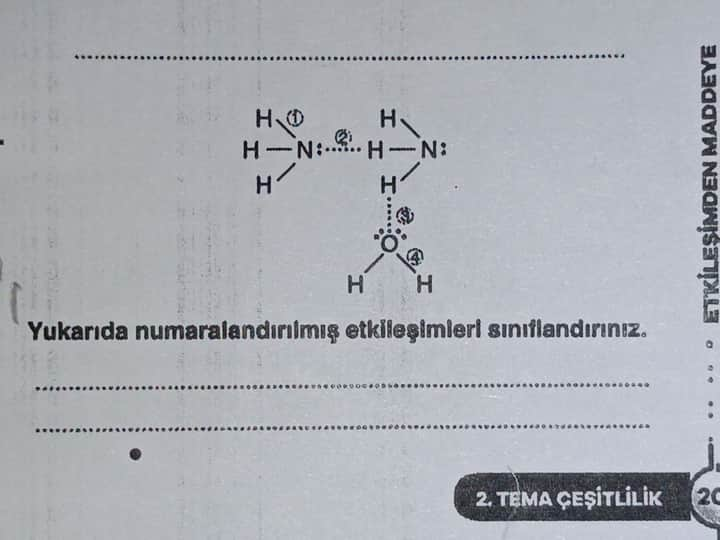
Yukarıda Gösterilen NH₃ (Amonyak) ve H₂O (Su) Moleküllerine Ait Etkileşimleri ve Lewis Yapılarını Açıklayınız
Cevap:
Aşağıdaki açıklamalar, amonyak ve su moleküllerinde görülen bağ yapısı, elektron düzenlenmesi, molekül geometrisi ve bunların sonucunda ortaya çıkan hidrojen bağları vb. etkileşimleri kapsar.
1) Lewis Yapıları
-
Amonyak (NH₃)
- Azot (N) atomunun değerlik elektron sayısı 5tir (2s²2p³).
- Bu elektronların 3 tanesi hidrojenlerle kovalent bağ, geriye kalan 2 elektron ise lone pair (yalnız çift) oluşturur.
- Lewis yapısında merkezde azot üzerinde 1 tane yalnız elektron çifti, azota bağlı 3 tane H görülür.
-
Su (H₂O)
- Oksijen (O) atomunun değerlik elektron sayısı 6dır (2s²2p⁴).
- Bu elektronların 2 tanesi hidrojenlerle kovalent bağ, geriye kalan 4 elektron ise 2 tane yalnız çift (lone pair) oluşturur.
- Lewis yapısında merkezde oksijen üzerinde 2 tane yalnız elektron çifti, oksijene bağlı 2 tane H bulunur.
2) Molekül Geometrisi
-
Amonyak (NH₃)
- Azot atomu etrafında 3 bağ (N–H) ve 1 yalnız çift vardır. Bu, trigonal piramidal (üçgensel piramidal) bir geometri oluşturur.
- Bağ açısı ideal 109,5°’ten, yalnız çiftin itmesi sebebiyle yaklaşık 107°ye düşer.
-
Su (H₂O)
- Oksijen atomu etrafında 2 bağ (O–H) ve 2 yalnız çift vardır. Bu, bent (kırık, V-şekilli) bir geometri oluşturur.
- Bağ açısı ideal 109,5°’ten, yaklaşık 104,5°ye düşer.
3) Polarite ve Hidrojen Bağı
Hem NH₃ hem de H₂O polar moleküllerdir. Elektronegatiflik farkı nedeniyle azot ve oksijen atomu kısmi (δ–) yük kazanırken, hidrojenler kısmi (δ+) yük taşır.
- Hidrojen Bağı (H-Bağı)
- Su molekülleri arasında: \text{O-H}\dots\text{O}
- Amonyak molekülleri arasında: \text{N-H}\dots\text{N}
- Ayrıca su ve amonyak bir araya geldiğinde de oksijenin veya azotun üzerindeki yalnız çift, diğer moleküldeki hidrojenle etkileşerek hidrojen bağı oluşturabilir. Bu bağ, dipol-dipol etkileşiminden çok daha güçlü bir moleküller arası kuvvettir.
4) Özet Tablo
| Özellik | NH₃ (Amonyak) | H₂O (Su) |
|---|---|---|
| Merkez Atom | N | O |
| Değerlik Elektron Dizenimi | 2s²2p³ (5 değerlik e⁻) | 2s²2p⁴ (6 değerlik e⁻) |
| Lewis Yapısı | 1 Yalnız Çift, 3 Bağ | 2 Yalnız Çift, 2 Bağ |
| Molekül Geometrisi | Trigonal Piramidal | Bent (V-Şekilli) |
| Bağ Açısı (yaklaşık) | 107° | 104.5° |
| Moleküler Polarite | Polar | Polar |
| Moleküller Arası Etkileşim | Hidrojen Bağı, Dipol-Dipol, London | Hidrojen Bağı, Dipol-Dipol, London |
| Önemli Nokta | NÜzerinde 1 yalnız çift | O üzerinde 2 yalnız çift |
Kısaca:
- Her iki molekül de polar olduğu için hidrojen bağı en baskın etkileşim türüdür.
- Lewis yapılarında azot ve oksijenin üzerindeki yalnız çift elektronlar, hidrojen bağlarının temelini oluşturur.
- Bağ açıları, yalnız çiftlerin azot/oksijen üzerindeki itmesi sebebiyle ideal tetrahedral açıdan daha küçüktür.
Yukarıdaki şekilde numaralandırılmış etkileşimleri inceleyerek her birini tanımlayabiliriz. Genel olarak, bir molekül içindeki (intramoleküler) bağlar kovalent, iki farklı molekül arasında (intermoleküler) oluşan çekimler ise dipol-dipol, hidrojen bağı vb. şeklinde sınıflandırılır. Soru görselinde tipik olarak su (H₂O) ve amonyak (NH₃) moleküllerinin birbirleriyle kurduğu hidrojen bağları ve her bir molekülün kendi içindeki kovalent bağları gösterilir.
Aşağıda, olası numaralandırmalar ve açıklamaları örnek olarak verilmiştir (gerçek numaraların görseldeki sıra ile eşleştirilmesi gerekebilir):
-
N–H Bağı (Polar Kovalent)
– Amonyak (NH₃) molekülündeki azot (N) ile hidrojen (H) arasındaki bağdır. Elektronegatiflik farkı nedeniyle bu kovalent bağda N kısmen negatif (δ–), H kısmen pozitif (δ+) yük taşır. -
O–H Bağı (Polar Kovalent)
– Su (H₂O) molekülündeki oksijen (O) ile hidrojen (H) arasındaki kutuplu (polar) kovalent bağdır. Oksijenin elektronegatifliği daha yüksek olduğu için O kısmen negatif (δ–), H kısmen pozitif (δ+) olur. -
Hidrojen Bağı (N–H···O ya da O–H···N)
– Amonyak molekülünün kısmen pozitif (δ+) H atomu ile su molekülünün kısmen negatif (δ–) O atomu (ya da tersi durumda NH₃’nin N atomu ile H₂O’nun H atomu) arasında oluşur. Hidrojen bağları, polar kovalent bağla bağlanmış (N–H, O–H, F–H gibi) hidrojenin, başka bir moleküldeki yüksek elektronegatif atomun (N, O, F) üzerine çekilmesiyle doğan en güçlü dipol-dipol etkileşim türüdür. -
Lone Pair (Yalnız Elektron Çifti) Gösterimleri
– Şekilde N veya O üzerinde görülen serbest (bağ yapmamış) elektron çiftleri “lone pair” olarak adlandırılır. Serbest elektron çiftleri, hidrojen bağı oluşumunda etken bölgelerden biridir.
Bunların dışında, eğer numaralandırma başka bağ veya etkileşimleri (örneğin molekül içi kovalent bağlar veya moleküller arası zayıf Van der Waals kuvvetleri) gösteriyorsa, benzer şekilde şu şekilde sınıflandırabiliriz:
- Polar Kovalent Bağ: İki farklı elektronegatiflikte ametal arasındaki bağ (örneğin N–H, O–H).
- Apolar (Nonpolar) Kovalent Bağ: Elektronegatiflik farkı yok veya çok az ise (örneğin aynı element atomları arası bağ).
- İyonik Bağ: Metal + ametal arasında elektron alışverişine dayanan bağlar (bu sorudaki görselde pek yer almıyor).
- Hidrojen Bağı: N, O veya F ile kovalent bağ yapmış (N–H, O–H, F–H) hidrojenin diğer bir molekülün N, O veya F atomuna yaklaşması ile oluşan kuvvetli dipol-dipol etkileşimi.
- London (Van der Waals) / Dipol-Dipol: Polar moleküller arası dipol-dipol veya apolar moleküller arası anlık dipol-indüklenmiş dipol etkileşimleri.
Aşağıda bir özet tablo sunulmuştur:
| Numara | Bağ/Etkileşim Tipi | Örnek | Açıklama |
|---|---|---|---|
| 1 | Polar Kovalent Bağ | N–H (amonyak içinde) / O–H (su içinde) | Elektronegatiflik farkı yüksek, δ– ve δ+ yük dağılımı |
| 2 | Hidrojen Bağı (intermoleküler) | NH₃ ve H₂O molekülleri arasındaki H···O veya H···N | Kuvvetli bir dipol-dipol etkileşimi, H (δ+) ile N/O (δ–) arasında oluşur |
| 3 | Lone Pair | N veya O üzerinde bağ yapmamış elektron çifti | Hidrojen bağı oluşumuna katkı sağlar |
| 4 | (Varsa) Apolar Kovalent Bağ | Aynı element atomları arası (genelde bu görselde yok) | Elektronegatiflik farkı çok az veya sıfır |
Bu şekilde numaralandırılmış etkileşimler büyük ihtimalle molekül içi (N–H, O–H) polar kovalent bağları ve moleküller arası hidrojen bağlarını (NH₃ ↔ H₂O etkileşimi) göstermektedir. Yalnız elektron çiftleri de (lone pair) ayrıca belirtilir.
Yukarıda temel hâl elektron dizilimleri verilen X, Y, Z atomları ile ilgili sorular:
• X: 1s² 2s² 2p⁴
• Y: 1s² 2s² 2p⁵
• Z: 1s² 2s² 2p⁶ 3s¹
Bu dizilimlere göre:
- X oksijen (O, Z=8),
- Y flor (F, Z=9),
- Z sodyum (Na, Z=11) atomuna karşılık gelir.
a) X ile Z Arasında Oluşan Kararlı Bileşik ve Bağ Türü
- X (O) atomunun değerlik katmanında 6 elektron (2s² 2p⁴),
- Z (Na) atomunun değerlik katmanında 1 elektron (3s¹) bulunur.
Oksijen (O) oktetini tamamlayabilmek için 2 elektron almalıdır. Her bir sodyum (Na) atomu 1 elektron vererek artı yüklü iyon (Na⁺) hâline gelir. Oksijen (O) eksi yüklü iyon (O²⁻) hâline gelmesi için 2 elektron kazanır. Böylece 2 Na atomu, 1 O atomuna elektron vererek Na₂O bileşiğini oluşturur.
- Bileşik Formülü: Na₂O
- Bağ Türü: İyonik (metal + ametal)
b) X ile Y Arasında Oluşan XY₂ Bileşiğinin Lewis Yapısı ve Kısmi Yükler
- X (O) ile Y (F) atomlarının oluşturduğu XY₂ formülü, OF₂ (Oksijen diflorür) şeklindedir.
- Oksijenin değerlik katmanında 6 elektron, her bir flor atomunun ise 7 değerlik elektronu vardır.
- Lewis yapısında O merkezi atom olacak şekilde iki tekli bağ ile iki F atomuna bağlanır. Böylece:
- Oksijen (O) 2 bağ ve 2 yalnız (lone) elektron çifti bulundurur.
- Her flor (F) atomu, O’ya tek bağla bağlanır ve toplam 3 yalnız çift taşıyarak oktetini tamamlar.
Lewis yapısı (basitleştirilmiş gösterim):
F : : F
| |
: O :----------: O :
|
Burada “:” noktaları elektron çiftlerini temsil eder.
- Kısmi Yük Dağılımı (δ⁺, δ⁻)
Flor (F) elementi periyodik tabloda en yüksek elektronegatifliğe sahip elementtir. Dolayısıyla flor atomları elektronları kendilerine doğru daha fazla çeker.- Oksijen (O) üzerinde kısmi pozitif yük (δ⁺)
- Her bir flor (F) üzerinde kısmi negatif yük (δ⁻) bulunur.
Özet Tablo
| Atom | Elektron Dizilimi | Element | Kombinasyon | Bağ Türü | Bileşik Formülü |
|---|---|---|---|---|---|
| X | 1s² 2s² 2p⁴ | Oksijen (O) | Z (Na) ile (metal + ametal) | İyonik | Na₂O |
| Y | 1s² 2s² 2p⁵ | Flor (F) | X (O) ile (ametal + ametal) | Kovalent | OF₂ (XY₂) |
| Z | 1s² 2s² 2p⁶ 3s¹ | Sodyum (Na) | - | - | - |
- X ile Z (Na₂O): İyonik bağ
- X ile Y (OF₂): Kovalent bağ (Lewis yapısında O merkez, F atomları δ⁻, O atomu δ⁺)
Yukarıdaki şekilden anlaşıldığı üzere numaralandırılmış etkileşimler, molekül içi (kovalent) ve moleküller arası (hidrojen bağı vb.) etkileşimleri göstermektedir. Aşağıdaki sınıflandırma tipik bir NH₃ (amonyak) ve H₂O (su) örneğini yansıtır:
- (1) N–H bağları (Amonyak içi)
- Amonyaktaki azot ile hidrojen arasındaki kutup*lu kovalent bağdır (polar kovalent bağ).
- (2) H…N (kesikli çizgi)
- Farklı amonyak molekülleri (veya amonyak-su) arasında azotun üzerindeki yalnız elektron çifti ile başka bir moleküldeki H arasında oluşan hidrojen bağıdır (moleküllerarası).
- (3) H…O (kesikli çizgi)
- Suyun (O) üzerindeki yalnız elektron çifti ile amonyaktaki (veya suyun kendi H’si) hidrojen arasında oluşan hidrojen bağıdır (moleküllerarası).
- (4) O–H bağları (Su içi)
- Suyun içinde oksijen ile hidrojen arasındaki kutup*lu kovalent bağdır (polar kovalent bağ).
Bu şekilde, (1) ve (4) numaralı bağlar molekül içi kovalent bağlar, (2) ve (3) numaralı kesikli çizgiler ise moleküllerarası hidrojen bağları olarak sınıflandırılır.
Özet Tablo
| Numara | Etkileşim Türü | Açıklama |
|---|---|---|
| (1) | Polar Kovalent Bağ (N–H) | Amonyak molekülündeki azot-hidrojen bağları |
| (2) | Hidrojen Bağı (H…N) | Farklı NH₃ molekülleri (veya NH₃–H₂O) arasındaki etkileşim |
| (3) | Hidrojen Bağı (H…O) | Amonyak ile su veya su molekülleri arasındaki etkileşim |
| (4) | Polar Kovalent Bağ (O–H) | Su molekülündeki oksijen-hidrojen bağları |
Yukarıdaki şekilde numaralandırılmış bağlar/etkileşimler tipik olarak şu şekilde sınıflandırılır:
-
(1) N–H (kovalent bağ)
Burada azot (N) ile hidrojen (H) arasında ortak elektron paylaşımı söz konusudur. Bu, molekül içi (intramoleküler) kovalent bir bağdır. -
(2) Noktalı çizgi ile gösterilen N···H–O (hidrojen bağı)
Azot üzerindeki yalnız (lone) elektron çiftinin, oksijene bağlı hidrojenin kısmi pozitif (δ⁺) merkeziyle etkileşmesi sonucunda hidrojen bağı (zayıf ancak en güçlü ikincil etkileşim) oluşur. Bu bağ genellikle moleküller arası (intermoleküler) sınıfa girer. -
(3) O–H (kovalent bağ)
Oksijen ile hidrojen arasındaki molekül içi (intramoleküler) kovalent bağdır. Oksijen 2 elektron, hidrojen 1 elektron getirerek bağ oluşturur. -
(4) Dipol-dipol ve/veya elektrostatik çekim
Oksijenin daha elektronegatif olması nedeniyle kısmi negatif (δ⁻) yük taşıması ve azot/hidrojen üzerinde kısmi pozitif (δ⁺) yük bulunması, dipol-dipol etkileşimini destekler. Bu etkileşim de moleküller arası bir zayıf etkileşimdir.
Özet Tablo
| Numara | Etkileşim Türü | Açıklama |
|---|---|---|
| (1) | Kovalent Bağ (N–H) | Azot ile hidrojen arasında paylaşılmış elektron çifti (intramoleküler) |
| (2) | Hidrojen Bağı (N···H–O) | Azotun yalnız elektron çifti ile O–H üzerindeki hidrojenin etkileşimi (intermoleküler) |
| (3) | Kovalent Bağ (O–H) | Oksijen ile hidrojen arasında paylaşılmış elektron çifti (intramoleküler) |
| (4) | Dipol-Dipol / Elektrostatik Etkileşim | Kısmi negatif (O) ile kısmi pozitif (N–H) uçlar arasındaki çekim (intermoleküler) |
Bu sınıflandırma, genel olarak moleküller içi kovalent bağlar (N–H, O–H) ile moleküller arası zayıf etkileşimler (hidrojen bağları ve dipol-dipol) arasında yapılan ayrımı gösterir.