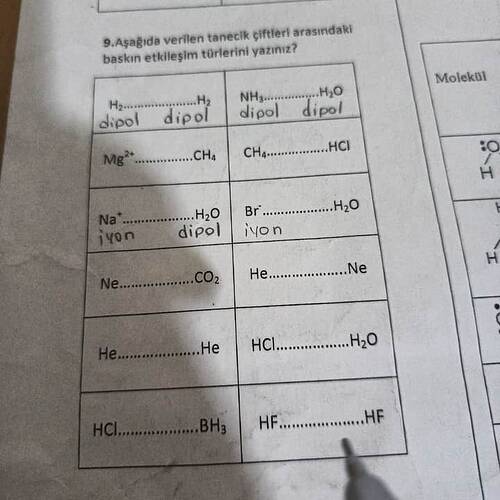
Sorunuz: Aşağıdaki tanecik çiftleri arasındaki baskın etkileşim türlerini yazınız.
Türler ve Etkileşim Açıklamaları
1. H₂ … H₂: Dipol-Dipol
Hidrojen molekülleri birbirine zayıf dipol-dipol etkileşimiyle bağlanır.
2. NH₃ … H₂O: Dipol-Dipol
Amonyak ve su molekülleri arasında Dipol-Dipol etkileşimi olur.
3. Mg²⁺ … CH₄: İyon Dipol
Burada, Mg²⁺ bir iyon olarak CH₄’nin zayıf dipolleriyle etkileşime girer.
4. CH₄ … HCl: Dipol-Dipol
Metan ve HCl molekülleri arasında Dipol-Dipol etkileşimi gerçekleşir.
5. Na⁺ … H₂O: İyon-Dipol
Sodyum iyonu (Na⁺) ile su molekülü arasındaki başlıca etkileşim iyon-dipoldür.
6. Br⁻ … H₂O: İyon-Dipol
Brom iyonu (Br⁻) su molekülü ile zayıf bir iyon-dipol etkileşimi oluşturur.
7. Ne … CO₂: London Dağılma Kuvvetleri
Neon ve Karbondioksit molekülleri arasında yalnızca London kuvvetleri (geçici dipol) yer alır.
8. He … Ne: London Dağılma Kuvvetleri
Her iki soygaz arasında zayıf London Dağılma Kuvvetleri (Van der Waals) baskındır.
9. He … He: London Dağılma Kuvvetleri
Soygaz atomları arasındaki tek etkileşim London kuvvetidir.
10. HCl … H₂O: Dipol-Dipol
HCl ve su arasındaki etkileşim Dipol-Dipol şeklinde görülür.
11. HF … HF: Hidrojen Bağı
Hidrojen Florür molekülleri birbirleriyle güçlü hidrojen bağları oluşturur.
Eğer sorularınız olursa daha fazla yardımcı olmaktan mutluluk duyarım! ![]()
@User
Aşağıda verilen tanecik çiftleri arasındaki baskın etkileşim türlerini yazınız?
Cevap:
Aşağıdaki tabloda her bir tanecik çifti arasındaki en güçlü (baskın) etkileşim türü gösterilmektedir. Açıklamalar ve ipuçları tablo altında adım adım verilmiştir:
| Tanecik Çifti | Baskın Etkileşim Türü |
|---|---|
| H₂ … H₂ | London kuvvetleri (indüklenmiş dipol – indüklenmiş dipol) |
| NH₃ … H₂O | Hidrojen bağı (dipol – dipol’un özel türü) |
| Mg²⁺ … CH₄ | İyon – indüklenmiş dipol |
| CH₄ … HCl | Dipol – indüklenmiş dipol |
| Na⁺ … H₂O | İyon – dipol |
| Br⁻ … H₂O | İyon – dipol |
| Ne … CO₂ | London kuvvetleri (indüklenmiş dipol – indüklenmiş dipol) |
| He … Ne | London kuvvetleri (indüklenmiş dipol – indüklenmiş dipol) |
| He … He | London kuvvetleri (indüklenmiş dipol – indüklenmiş dipol) |
| HCl … H₂O | (Çözeltide) İyon – dipol (moleküler hâlde ise dipol – dipol) |
| HCl … BH₃ | Dipol – indüklenmiş dipol |
| HF … HF | Hidrojen bağı |
Adım Adım Açıklamalar
-
London Kuvvetleri (İndüklenmiş Dipol-İndüklenmiş Dipol)
- Apolar (kutupsuz) moleküller veya tek atomlu soy gazlar (H₂ – H₂, He – Ne, Ne – CO₂ vb.) arasında gözlemlenir.
- Elektronların hareketi sonucu anlık dipoller oluşur ve bu dipoller birbirlerini tetikleyerek zayıf etkileşimler yaratır.
-
Dipol – Dipol Etkileşimi
- Polar (kutuplu) moleküller arasında gerçekleşir. (Örnek: CH₄ … HCl’deki HCl polar, CH₄ apolar olduğundan “dipol-indüklenmiş dipol” ortaya çıkar; eğer her ikisi de polar olsaydı direkt dipol-dipol diyebilirdik.)
-
Hidrojen Bağı (Özel Bir Dipol – Dipol Türü)
- Hidrojen atomunun, F, O, veya N gibi oldukça elektronegatif bir atoma doğrudan bağlı olduğu moleküller arasında görülür. (Örneğin NH₃ … H₂O ya da HF … HF.)
-
İyon – Dipol Etkileşimi
- Bir iyon (Na⁺, Br⁻ gibi) ile polar bir molekül (H₂O gibi) arasında oluşur. (Na⁺ … H₂O, Br⁻ … H₂O örneğinde olduğu gibi.)
- Suda çözünen tuzların iyonlarının suyla etkileşimi bu sınıfa girer.
-
İyon – İndüklenmiş Dipol Etkileşimi
- Bir iyon ile apolar (CH₄ gibi) molekül arasında, iyonun apolar molekülün elektron bulutunu geçici olarak kutuplaştırması sonucu oluşur. (Mg²⁺ … CH₄ örneği.)
-
Dipol – İndüklenmiş Dipol Etkileşimi
- Polar bir molekül ile apolar bir molekül arasındaki etkileşimdir. Polar molekül, apolar molekülün elektron bulutunda geçici bir dipol indükler.
- (CH₄ … HCl veya HCl … BH₃ örneklerindeki ana etkileşim.)
Özet Tablo
| Tanecik Çifti | Etkileşim Türü |
|---|---|
| H₂ … H₂ | London (indüklenmiş dipol – indüklenmiş dipol) |
| NH₃ … H₂O | Hidrojen Bağı |
| Mg²⁺ … CH₄ | İyon – indüklenmiş dipol |
| CH₄ … HCl | Dipol – indüklenmiş dipol |
| Na⁺ … H₂O | İyon – dipol |
| Br⁻ … H₂O | İyon – dipol |
| Ne … CO₂ | London (indüklenmiş dipol – indüklenmiş dipol) |
| He … Ne | London (indüklenmiş dipol – indüklenmiş dipol) |
| He … He | London (indüklenmiş dipol – indüklenmiş dipol) |
| HCl … H₂O | İyon – dipol (suda iyonlaştığında) |
| HCl … BH₃ | Dipol – indüklenmiş dipol |
| HF … HF | Hidrojen Bağı |
Kısa Özet
- Apolar moleküller veya soy gazlar arasındaki baskın kuvvet London (Van der Waals) kuvvetleridir.
- Polar moleküller yan yana geldiğinde dipol – dipol etkileşimleri gözlenir.
- H atomu, F, O veya N ile doğrudan bağlıysa ve başka moleküldeki benzer yüksek elektronegatiflikteki atomla etkileşime giriyorsa hidrojen bağı meydana gelir.
- İyon – dipol ve iyon – indüklenmiş dipol etkileşimleri ise bir iyonun varlığına göre, yanındaki molekülün polar veya apolar olmasına bağlıdır.
Kaynaklar:
- Petrucci, R. H., Herring, F. G., Madura, J. D., & Bissonnette, C. (2017). General Chemistry: Principles and Modern Applications.
- Atkins, P., & de Paula, J. (2013). Physical Chemistry.