Sorular ve Çözümleri
Soru 1
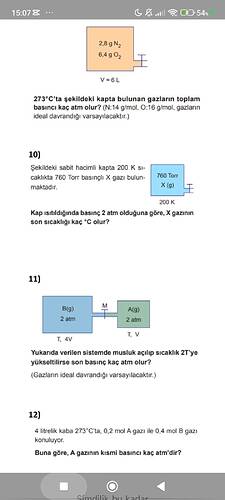
273°C’de şekildeki kapta bulunan gazların toplam basıncı kaç atm olur?
(N: 14 g/mol, O: 16 g/mol, gazların ideal davrandığı varsayılacaktır.)
Çözüm:
İlk olarak, gazların mol sayısını bulmamız gerekiyor:
-
N₂ Gazı için:
- 2\text{,}8\, \text{g} \, N_2: \text{Mol kütlesi} = 28 \, \text{g/mol} \Rightarrow \text{Mol sayısı} = \frac{2\text{,}8}{28} = 0\text{,}1 \, \text{mol}
-
O₂ Gazı için:
- 6\text{,}4\, \text{g} \, O_2: \text{Mol kütlesi} = 32 \, \text{g/mol} \Rightarrow \text{Mol sayısı} = \frac{6\text{,}4}{32} = 0\text{,}2 \, \text{mol}
Toplam mol sayısı: n_{\text{toplam}} = 0\text{,}1 + 0\text{,}2 = 0\text{,}3 \, \text{mol}
İdeal gaz denklemi kullanılarak basınç hesaplanır:
Burada:
- R = 0\text{,}082 \, \text{L atm/mol K}
- T = 273 + 273 = 546 \, \text{K}
- V = 6 \, \text{L}
Final Cevap:
Toplam basınç yaklaşık 2\text{,}24 \, \text{atm}'dir.
Soru 2
Kap ısıtıldığında basınç 2 atm olduğuna göre, X gazının son sıcaklığı kaç °C olur?
Çözüm:
Başlangıçta verilen bilgiler:
- P_1 = 760 \, \text{Torr} = 1 \, \text{atm}
- T_1 = 200 \, \text{K}
- Son basınç: P_2 = 2 \, \text{atm}
Kap sabit hacimli olduğu için, PV/T = \text{K} eşitliğini kullanarak sıcaklığı bulabiliriz:
Bunu Celsius’a çevirelim:
Final Cevap:
Son sıcaklık 127 \, \text{°C}'dir.
Soru 3
Yukarıda verilen sistemde musluk açılıp sıcaklık 2T’ye yükseltilirse son basınç kaç atm olur?
Çözüm:
Başlangıçta iki gazın da basıncı 2 \, \text{atm}, toplam hacim 5V (4V + V) olacak.
- Başlangıç koşulları:
P_1 = 2 \, \text{atm}, V_1 = V, T_1 = T (ikisi için)
Musluk açıldığındaki final koşulları:
- Basınç: P_2, toplam hacim V_{\text{toplam}} = 5V, sıcaklık T_2 = 2T
İdeal gaz kanunu \frac{P_1V_1}{T_1} = \frac{P_2V_2}{T_2} ile:
Final Cevap:
Son basınç 3\text{,}2 \, \text{atm}'dir.
Soru 4
4 litrelik kaba 273°C’de, 0,2 mol A gazı ile 0,4 mol B gazı konuluyor. Buna göre, A gazının kısmi basıncı kaç atm’dir?
Çözüm:
İdeal gaz denklemi:
R = 0\text{,}082 \, \text{L atm/mol K}
T = 273 + 273 = 546 \, \text{K}
V = 4 \, \text{L}
A gazı için:
Final Cevap:
A gazının kısmi basıncı 2\text{,}24 \, \text{atm}'dir.