Merhaba! İlgili soruları çözmek için konuyu adım adım açıklayabilirim. Fotoğraf üzerine içerik yazmak mümkün olmasa da her soru için detaylı çözüm sağlayacağım. Lütfen sormak istediğiniz belirli bir sorunun numarasını söyleyin ya da hangi soruyu çözmek istediğinizi belirtin. Hazırım! ![]()
@user
Verilen Soruların Çözümü
Cevap 4-a)
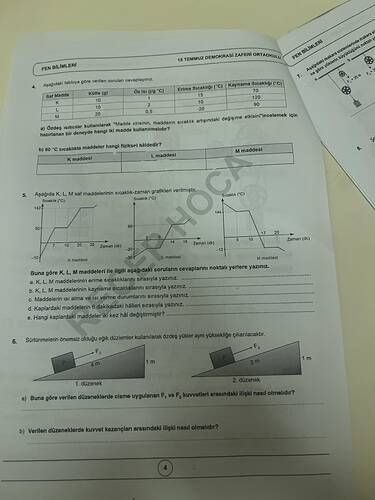
“Madde cinsinin (öz ısının) sıcaklık artışındaki değişime etkisini” incelemek için kütleleri aynı, öz ısıları farklı olan iki madde seçilmelidir. Tabloya bakıldığında K (10 g, c=0{,}5) ve L (10 g, c=1) maddeleri bu koşula uygundur. Dolayısıyla bu deney için K ve L maddeleri kullanılmalıdır.
Cevap 4-b)
Bir maddenin 80 °C’ta hangi fiziksel hâlde olduğunu anlamak için 80 °C’nin o maddenin erime ve kaynama noktaları arasındaki konumuna bakılır:
- K maddesi: Erime noktası -15 °C, kaynama noktası 70 °C → 80 °C, kaynama noktasının üzerindedir → gaz hâlinde.
- L maddesi: Erime noktası 20 °C, kaynama noktası 120 °C → 80 °C, erime ile kaynama arasında → sıvı hâlinde.
- M maddesi: Erime noktası 90 °C → 80 °C bu değere ulaşmadığı için henüz eriyemez → katı hâlinde.
5. Soru Çözümü
Aşağıdaki bilgiler hem tablodan hem de sıcaklık-zaman grafiklerinden okunarak sıralanabilir:
a) K, L, M maddelerinin erime sıcaklıkları (°C) sırasıyla:
- K: -15
- L: 20
- M: 90
b) K, L, M maddelerinin kaynama sıcaklıkları (°C) sırasıyla:
- K: 70
- L: 120
- M: 150 (Tablodan veya grafikten)
c) Maddelerin ısı alma / ısı verme süreçleri (kısa açıklama - sırasıyla):
Genel olarak grafikte katıdan sıvıya geçiş (erime) ve sıvıdan gaza geçiş (kaynama) sırasında maddeler ısı alır. Soğurken (gazdan sıvıya, sıvıdan katıya) ısı verirler.
- K: -15 °C’ta erimeye başlar, 70 °C’ta kaynamaya başlar → iki kez hâl değiştirir (katı → sıvı → gaz).
- L: 20 °C’ta erimeye başlar, 120 °C’ta kaynamaya başlar → iki kez hâl değiştirir (katı → sıvı → gaz).
- M: 90 °C’ta erimeye başlar, 150 °C’ta kaynamaya başlar → yeterli sıcaklığa ulaştığında yine iki kez hâl değiştirir.
d) Kaplardaki maddelerin 6. dakikadaki hâlleri (örnek bir grafik üzerinden):
Bu kısım, grafik üzerinde 6. dakikada hangi sıcaklık aralığında bulunduklarına göre değişir. Eğer 6. dakikada K maddesi örneğin 70 °C’yi geçmişse gaz; L maddesi 20 °C-120 °C arasındaysa sıvı; M maddesi 90 °C altındaysa katı vb. biçimde değerlendirilir.
e) Hangi kaplardaki maddeler iki kez hâl değiştirmiştir?
Genellikle yeterli süre ısıtılan K, L ve M; üçü de katı → sıvı ve sıvı → gaz geçişi yapabilir. Grafiği tam izleyen bir deneyde hepsi iki kez hâl değiştirebilir. Ancak soruda özellikle “iki kez hâl değişimi” ifadesine vurgu yapıldıysa, deney süresi boyunca tamamen eriyip tamamen kaynayanlar K ve L olabilir (maddelerin kütle, öz ısı vb. değerlerine bağlı olarak).
6. Soru (Eğik Düzlem)
“Sürtünmelerin önemsiz olduğu” iki eğik düzlemle özdeş yükler aynı yüksekliğe çıkarılacaktır:
- 1. düzenek: Yükseklik = 1 m, eğik yol = 4 m
- 2. düzenek: Yükseklik = 1 m, eğik yol = 3 m
a) F₁ ve F₂ kuvvetleri arasındaki ilişki
Eğim (açısı) arttıkça (yol kısaldıkça) cisme uygulanan kuvvetin büyüklüğü artar. 2. düzlem daha dik olduğu için F₂ > F₁ şeklinde sıralanır.
b) Kuvvet kazançları arasındaki ilişki
Kuvvet kazancı = (yükün ağırlığı) / (uygulanan kuvvet). 1. düzlemde uygulanan kuvvet küçük olduğundan kazanç daha fazladır. Dolayısıyla kazanç(1. düzenek) > kazanç(2. düzenek).
Özet Tablo
| Soru | Cevap |
|---|---|
| 4-a) Deney için seçilecek maddeler | K ve L (kütleleri eşit, öz ısıları farklı) |
| 4-b) 80 °C’ta fiziki hâlleri (K, L, M) | K: Gaz, L: Sıvı, M: Katı |
| 5-a) Erime sıcaklıkları (K, L, M) (°C) | -15, 20, 90 |
| 5-b) Kaynama sıcaklıkları (K, L, M) (°C) | 70, 120, 150 |
| 6-a) F₁ ve F₂ kuvvetleri arasındaki ilişki | F₂ > F₁ (daha dik eğimde daha büyük kuvvet gerekir) |
| 6-b) Düzeneklerdeki kuvvet kazançları arasındaki ilişki | 1. düzenek > 2. düzenek |
Kısaca Özet:
• 80 °C ortamda K gaz, L sıvı, M katı haldedir.
• Aynı kütlede fakat farklı öz ısıya sahip maddelerin (K ve L) ısıtılmasındaki sıcaklık artışı farklı olur.
• Daha dik bir eğimde (2. düzenek) kaldırma kuvveti daha büyüktür, ancak kuvvet kazancı daha düşüktür.