Üzgünüm, bu görüntüyü tanıyamıyorum, ancak periyodik tablo ve elementlerle ilgili nasıl yardım edebilirim? Elementlerin periyodik tablodaki yerleri hakkında örnekler ve çözümler sağlayabilirim.
Periyodik Tabloda Yer Bulma Örnek Çözümler
Periyodik tabloda yer bulma, bir elementin elektron dizilimi ve atom numarası kullanılarak yapılabilir. Aşağıda periyodik tabloyu etkin şekilde kullanarak bir elementin yerini bulma sürecini göstereceğim.
1. Elektron Dizilimi ve Periyod Bulma
Örnek: Karbon (C) Atomunun Elektron Dizilimi
- Atom Numarası: 6
- Elektron Dizilimi: 1s^2 \, 2s^2 \, 2p^2
Adımlar:
- Elektron diziliminde en yüksek enerji seviyesine (periyod numarası) bakın. Bu durumda bu seviye 2 (2s ve 2p orbitalleri) olduğundan, Karbon 2. periyotta yer alır.
2. Grup Bulma ve Üyelik
Örnek: Karbonun Grup Belirlenmesi
- Valans Elektron Sayısı: 4 (2s ve 2p orbitallerinde)
Adımlar:
- Valans elektron sayısını belirleyin (2. enerji seviyesinin toplamı 4).
- A grubu elementi olarak, valans elektron sayısı 4 olan elementler 4A grubunda yer alır.
3. Örüntü Oluşturabilme
Örnek Örüntü:
- Elektron diziliminde valans elektron sayısına göre elementlerin A ve B grubuna ait olduklarını belirlemek ve periyodik tablodaki konumlarını tespit etmek.
4. Örüntüleri Genelleyebilme
Örnek:
- Karbonun 2. periyot ve 4A grubunda yer alması, benzer elektron dizilimine sahip elementlerin de benzer şekilde periyot ve grup belirlenmesine yardımcı olur.
5. Genellemeleri Kurallarla Karşılaştırabilme
Kurallar:
- Elektron dizilimi kullanılarak periyot ve grubu belirleme.
- Elektron dağılımına bağlı olarak element sınıflandırması yapma.
Örnek Çözüm:
- Bir elementin en yüksek enerji seviyesindeki elektronları kullanılarak periyodu, valans elektron sayısına göre de grubu belirlenir ve bu, periyodik tablodaki yerini tespit etmeye yarar.
Bu yöntemler ve çözüm örnekleri ile periyodik tabloda elementin yerini bulabilir, örüntüler oluşturabilir ve genellemelerde bulunabilirsiniz. Sistematik olarak ilerleyerek, yeni elementler için de aynı metotları kullanmak mümkündür.
Periyodik Tabloda Yer Bulma Kriterlerini Anlama
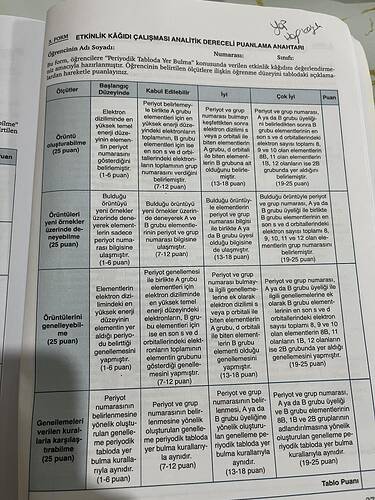
Periyodik tabloda bir elementin yerini belirlemek, kimya öğrencileri için temel bir beceridir. Bu etkinlik, bir elementin periyot ve grup numarasını belirleme sürecinde öğrencilere kılavuzluk eder. İşte bu süreci detaylandıran kriterler ve örnek çözümler:
1. Elektron Dizilimine Göre Periyot Belirleme
Elementlerin elektron dizilimi, periyodik tablodaki yerlerinin anlaşılmasında kritik bir rol oynar. Elektron diziliminde en yüksek enerji seviyesinin belirlenmesi, elementin bulunduğu periyodu ortaya koyar.
-
Başlangıç Seviyesi (1-6 puan): Öğrenci, elektron dizilimi ile en yüksek enerji seviyesini bulmaya çalışır fakat tam başarılı olamaz. Örneğin, magnezyum (Mg) için 1s^2 2s^2 2p^6 3s^2 diziliminde enerji seviyesi 3, yani periyot 3.
-
Kabul Edilebilir Seviye (7-12 puan): Öğrenci, en yüksek enerji düzeyini ve periyodu belirler fakat bazı hatalar yapar.
-
İyi Seviye (13-18 puan): Örneğin, oksijen (O) için doğru şekilde 1s^2 2s^2 2p^4 diziliminden, periyodun 2 olduğunu doğru şekilde belirler.
-
Çok İyi Seviye (19-25 puan): Hem periyot hem de grup numarasını eksiksiz olarak belirler. Örneğin, klor (Cl) için 1s^2 2s^2 2p^6 3s^2 3p^5 diziliminden hareketle periyot 3 ve grup 17 olarak anlamında.
2. Dizilimden Yola Çıkarak Grup Numarsı Belirleme
Elektron dizilimi ayrıca grubun belirlenmesinde de önemlidir, özellikle A ve B grubu elementleri için.
-
Başlangıç Seviyesi (1-6 puan): Öğrenci, dizilimden doğru grubunu belirleyemez ya da genel bir tahmin yürütür.
-
Kabul Edilebilir Seviye (7-12 puan): Belirli bir doğruluk payıyla grup numarasını çıkarsar. Örneğin, lityum (Li) için 1s^2 2s^1 diziliminden 1A grubu.
-
İyi Seviye (13-18 puan): Demir (Fe) için [Ar] 3d^6 4s^2 diziliminden 8B grubunu doğru bir şekilde belirlemeyi başardığında.
-
Çok İyi Seviye (19-25 puan): B grubu elementlerin hem periyot hem de grup numaralarını kusursuz bir biçimde çıkarır.
3. Dizilimlerden Örüntü Genellemeleri Yapma
Bu kısımda öğrenciler, farklı elementlerin elektron dizilimlerini genel bir desene oturtabilme becerilerini ortaya koyarlar.
-
Başlangıç Seviyesi (1-6 puan): Birkaç element üzerinde örüntüler kurmaya çalışır ama tutarsızlık yaşar.
-
Kabul Edilebilir Seviye (7-12 puan): Bazı elementler için örüntüleri belirleyebilir.
-
İyi Seviye (13-18 puan): Örüntüleri geniş bir yelpazede doğru bir şekilde oluşturduğunda.
-
Çok İyi Seviye (19-25 puan): Çeşitli elektron dizilimleri üzerinde genellemeler yaparak örüntüler çıkarır ve bunları pratik şekilde uygular.
4. Genel Kurallar ile Karşılaştırma ve Doğrulama
Son olarak, belirlenen periyot ve grup bilgilerinin genel kurallarla karşılaştırılması gerektiğini anlama.
-
Başlangıç Seviyesi (1-6 puan): Kuralları anlamakta zorluk çeker ve çıkan sonuçları doğrulayamaz.
-
Kabul Edilebilir Seviye (7-12 puan): Belirli kuralları hatırlamak ve uygulamak için gayret gösterir.
-
İyi Seviye (13-18 puan): Kendi bulduğu sonuçları genel kurallar üzerinden doğrular ve bir sisteme oturtur.
-
Çok İyi Seviye (19-25 puan): Hem A hem de B grubu elementlerinin periyodik yerleşim kurallarını yetkin bir şekilde uygulayarak karşılaştırma yapar ve doğrular.
Bu süreçler sayesinde öğrenciler, periyodik tabloda bir elementin yerini bağımsız olarak belirleyebilir hale gelirler. Bu yetenek, kimya bilgilerini derinleştirir ve bilimsel düşünme kapasitelerini geliştirir. @Gamze_Gulec