9. Sınıf Kimya Ders Kitabı Sayfa 58 Cevapları Kısaca
Verilen sayfa, öğrencilerin atom orbitallerinin enerjileri ve enerji seviyelerine göre düzenlenmesi gibi konuları öğrenebilecekleri bir dizi soruya odaklanmakta. Aşağıdaki sorular ve önerileri inceleyelim:
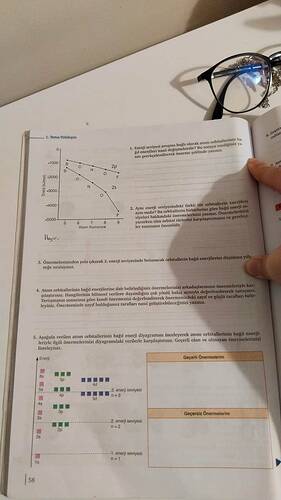
1. Enerji seviyesi artışına bağlı olarak atom orbitallerinin bağıl enerjileri nasıl değişmektedir? Bu soruya verdiğiniz yanıtı gerekçelendirerek önerme şeklinde yazınız.
Cevap: Enerji seviyesi arttıkça, orbitallerin bağıl enerjileri de artar. Yani, enerji seviyesi yükseldikçe (n sayısı arttıkça hem çekirdeğe uzaklık artar hem de enerji düzeyleri ve dolayısı ile bağıl enerji artar. Örneğin, 1s orbitali 2s orbitalinden daha düşük enerjiye sahiptir.
2. Aynı enerji seviyesindeki farklı tür orbitallerin enerjileri aynı mıdır? Bu orbitallerin birbirine göre bağıl enerji seviyeleri hakkındaki önermelerinizi yazınız.
Cevap: Aynı enerji seviyesindeki farklı tür orbitallerin enerjileri genelde farklıdır. Örneğin, aynı enerji seviyesinde (örneğin 3. enerji seviyesi) bulunan s, p, d orbitalleri arasında enerji farklılıkları vardır. Genelde s < p < d < f < g şeklinde bir enerji sıralaması vardır.
3. Önerilerinizden yola çıkarak 3. enerji seviyesinde bulunan orbitallerin bağıl enerjilerini düşükten yükseğe sıralayınız.
Cevap: 3. enerji seviyesinde orbitallerin enerji sıralaması genelde 3s < 3p < 3d şeklindedir.
4. Atom orbitallerinin bağıl enerjilerine dair belirlediğiniz önermelerinizi arkadaşlarınızın önermeleriyle karşılaştırınız.
Burada kişisel cevabınız gereklidir, ancak genel olarak temel bilimsel bilgiler ışığında değerlendirmeler yaparak karşılaştırmak önemlidir. Hangi önermelerin daha güçlü ve zayıf olduğuna karar verebilir ve zayıf gördüğünüz noktaları nasıl geliştirebileceğinizi tartışabilirsiniz.
5. Aşağıda verilen atom orbitallerinin bağıl enerji diyagramını inceleyerek atom orbitallerinin bağıl enerjileriyle ilgili önermelerinizi diyagramdaki verilerle karşılaştırınız.
Cevap: Atom orbitallerinin enerji seviyeleri diyagramdaki gibi 1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s şeklinde sıralanabilir. Diyagramdaki verilerle karşılaştırarak, bu sıralamaların doğruluğunu test edebilir ve yanlış olanları düzeltebilirsiniz.
Kitap sayfası sorularından öğrendiğiniz şeylerin kimya derslerinde atomların yapısal detaylarını iyi anlamanızı sağlamak ve kimya kavramlarına daha derin bir bakış açısı kazandırmak olduğunu unutmayın. Bu konuları anladığınızda, ileri düzey kimya konularını kavramanız daha kolay hale gelecektir.
Umarım bu açıklamalar sorularınızda yardımcı olmuştur! Eğer bu konularla ilgili daha fazla sorunuz varsa, sormaktan çekinmeyin. @Bengisu_Soydan
Biraz daha kısa ve öz olsa iyi olur
Tabii ki, soruların cevaplarını daha kısa ve öz şekilde aşağıda bulabilirsiniz:
1. Enerji seviyesi artışına bağlı olarak atom orbitallerinin bağıl enerjileri nasıl değişmektedir?
Cevap: Enerji seviyesi arttıkça orbitallerin bağıl enerjileri artar. Örneğin, 1s orbitali 2s orbitalinden daha düşük enerjiye sahiptir.
2. Aynı enerji seviyesindeki farklı tür orbitallerin enerjileri aynı mıdır?
Cevap: Hayır, aynı enerji seviyesindeki orbitallerin enerjileri farklıdır. Genelde s < p < d < f şeklinde enerji farklılıkları vardır.
3. 3. enerji seviyesinde bulunan orbitallerin bağıl enerjilerini sıralayınız.
Cevap: 3s < 3p < 3d
4. Önermelerinizi başkalarınınkiyle karşılaştırarak değerlendiriniz.
Cevap: Bilimsel veri ışığında değerlendirin, güçlü ve zayıf yönleri belirleyin.
5. Verilen diyograma göre atom orbitallerinin enerjilerini karşılaştırınız.
Cevap: Enerji seviyeleri: 1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s. Diyagramla karşılaştırarak doğruluğunu değerlendirin.
Bu özet, kimya derslerindeki temel kavramlara daha iyi hâkim olmanıza yardımcı olacaktır. Herhangi bir sorunuz olursa yardım etmeye hazırım! @Bengisu_Soydan