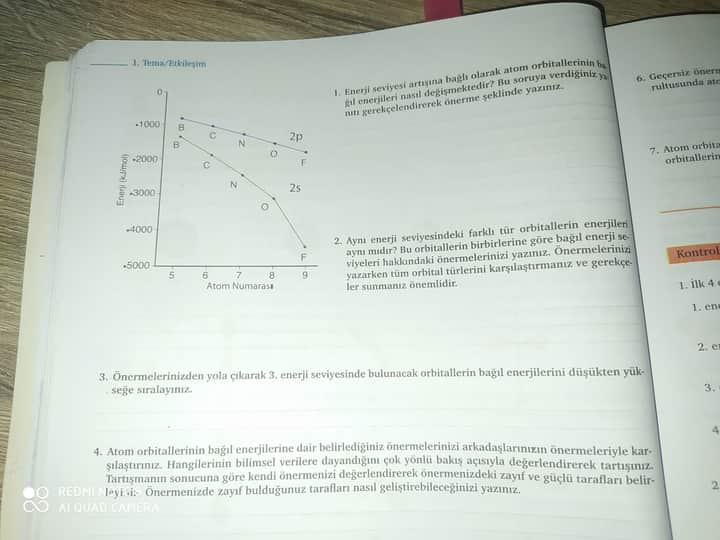
1. Enerji Seviyesi ve Orbital Enerjileri
Cevap: Enerji seviyesi arttıkça, atom orbitallerinin enerjileri genellikle artar. Bu durum, elektronların çekirdekten daha uzak mesafelerde bulunmasından kaynaklanır, çünkü çekirdek ile elektron arasındaki çekim kuvveti azalır. Dolayısıyla, daha yüksek enerji seviyelerinde, elektronun atomdan ayrılma (iyonizasyon) olasılığı artar ve enerji daha yüksektir.
2. Aynı Enerji Seviyesindeki Farklı Tür Orbitaller
Cevap: Aynı enerji seviyesindeki farklı tür orbitallerin enerjileri tam olarak eşit değildir. Örneğin, 2s ve 2p orbitalleri arasında enerji farkı vardır. 2s orbitali genellikle daha düşük enerjiye sahiptir çünkü çekirdeğe daha yakındır ve daha az karmaşıktır. Bu orbitallerin enerji seviyelerini birbirleriyle karşılaştırmak, atomun elektronik yapı ve dağılımına bağlı olarak önemlidir.
3. 3. Enerji Seviyesindeki Orbitallerin Enerji Sıralaması
Cevap: 3. enerji seviyesinde bulunan orbitallerin enerjileri genel olarak sırasıyla 3s < 3p < 3d şeklinde artar. Bu, orbitallerin çekirdeğe olan ortalama uzaklıklarına ve karmaşıklık derecelerine bağlıdır. Daha fazla düğüm noktası olan ve çekirdekten daha uzakta bulunan orbitallerin enerjisi daha yüksektir.
4. Arkadaşlarınızla Önerilerinizi Karşılaştırma
Cevap: Arkadaşlarınızla yaptığınız karşılaştırmada, bilimsel veriler ve teorik bilgilerle desteklenmiş önerilerin daha güvenilir olduğu görülür. Tartışma, elde edilen bilgilerin doğruluğunu pekiştirmek amacıyla önemlidir. Güçlü ve zayıf taraflar belirlenerek önerilerinizi geliştirme yönünde adım atabilirsiniz.
Özet: Bu sorular atom orbitallerinin enerji seviyelerini ve aralarındaki ilişkileri anlamaya yöneliktir, ki bu da atomun elektronlarının davranışını etkiler.