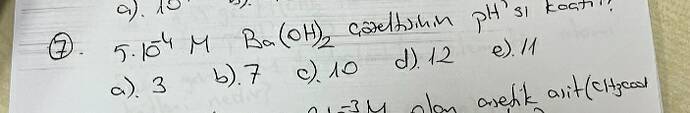Görüntüdeki soru, \(5 \times 10^{-4}\) M Ba(OH)₂ çözeltisinin pH değerini sormaktadır.
Cevap:
Ba(OH)₂, suda çözündüğünde aşağıdaki şekilde iyonlaşır:
\text{Ba(OH)}_2 \rightarrow \text{Ba}^{2+} + 2\text{OH}^-
Öyleyse, \(5 \times 10^{-4}\) M Ba(OH)₂ çözeltisi \(2 \times 5 \times 10^{-4} = 10^{-3}\) M OH⁻ iyonu içerir.
pOH’u bulmak için:
[
\text{pOH} = -\log [\text{OH}^-] = -\log (10^{-3}) = 3
]
pH’u bulmak için:
[
\text{pH} + \text{pOH} = 14 \implies \text{pH} = 14 - 3 = 11
]
Sonuç:
pH değeri 11’dir yani doğru cevap e) 11.