Sorunun Çözümü
Soruyu çözmek için öncelikle kimyasal tepkimeyi ve verilen miktarları analiz edelim.
Tepkime ve Mol Oranı:
Tepkime:
Bu tepkimeye göre 1 mol magnezyum (Mg) ile 0.5 mol oksijen (O(_2)) reaksiyona girerek 1 mol magnezyum oksit (MgO) oluşturuyor.
Verilenler:
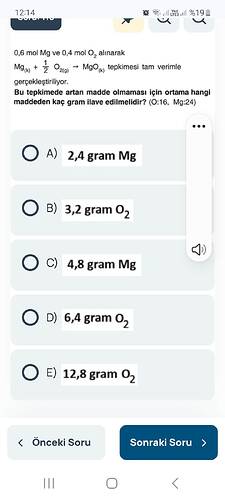
- Magnezyum (Mg): 0.6 mol
- Oksijen (O(_2)): 0.4 mol
- Daha fazla madde ekleyerek artan madde olmaması amaçlanıyor.
Adım 1: Tepkimeyi Analiz Etmek
Gerekli O(_2) miktarı:
0.6 mol Mg’nin tamamının reaksiyona girmesi için 0.6 (\times) 0.5 = 0.3 mol O(_2) gerekiyor.
Elimizdeki O(_2) miktarı: 0.4 mol
Bu durumda, Oksijen fazlalığı vardır, yani Mg eksiktir. O halde, daha fazla Mg ilave edilmelidir.
Adım 2: Mg’nin Hesaplanması
Oksijen (O(_2)) fazlalığını kullanarak gereken Mg miktarını hesaplayabiliriz. Elimizde 0.4 mol O(_2) olduğundan:
Ancak başlangıçta 0.6 mol Mg vardı. O halde ilave edilmesi gereken miktar:
Adım 3: Mg’yi Gram Cinsinden Hesaplama
Magnezyumun mol kütlesi (Mg): 24 gram/mol
İlave edilen Mg’nin gram cinsinden miktarı:
Sonuç:
Bu durumda artan madde olmaması için ortama 4.8 gram Mg ilave edilmelidir.
Cevap: C) 4,8 gram Mg
Tabloda Özet:
| Verilenler | Hesaplananlar | Sonuç |
|---|---|---|
| 0.6 mol Mg | Gerekli Mg: 0.8 mol | İlave Mg: 4.8 gram |
| 0.4 mol O(_2) | Gerekli O(_2): 0.3 mol | Fazla O(_2): Var |