Meva’nın sorusuna cevap vermek için, paylaşmış olduğu görsel üzerinde detaylı bir inceleme yapmam gerekiyor. Görselde kimyasal reaksiyona ait potansiyel enerji (P.E.) - tepkime koordinatı (T.K.) grafikleri ve entalpi değişimleri hakkında bir dizi sorular bulunduğu görülüyor.
Soruların Çözümüne Yönelik Adımlar
13. Soru: Tepkimenin Entalpi Değişimi
Tepkime:
Tepkimenin entalpi değişim formülü veriliyor: x = (… çeşitli enerji ifadeleri).
Bu tip sorularda şu adımlara dikkat etmek gerekiyor:
- Potansiyel enerji grafiği kullanılarak entalpiler hesaplanır.
- Tepkimenin başlangıç ve ürün enerjileri farkı hesaplanır.
- Eğer “x”, “y”, ve “z” gibi semboller kullanılmışsa tepkime enerjisi denklemi bu değerleri içerecek şekilde çözümlenir.
14. Soru: Gaz Miktarı Hesabı
Bu soruda verilen tepkime:
Verilen bilgiye göre:
- Tepkime sonucu açığa çıkan ısı: 0,2(x+2y).
- Hacim ve diğer detaylar: NK’deki gazın hacmi 13,44 L olarak verilmiş.
Formüller:
-
NK’de gazların mol hesabı:
n = \frac{V}{22,4}Burada V, gazın hacmidir ve 22,4 NK’deki molar hacmi temsil eder.
- Mole çevirme işlemiyle başlangıç gazı C_2H_4 miktarı hesaplanacaktır.
-
Mazot verilen diğer ısı değerleri veya grafikteki kısayollar kullanılmalı.
Yardımcı Olmam İçin Detay Verin
Eğer görsel daha büyük ve bölünmüş şekilde verilmesi gerekiyorsa veya spesifik bir kısmını çözmemi istiyorsanız, ayrıca belirtiniz. Soruların her iki kısmı için hesaplama adımlarını detaylı şekilde paylaşabilirim.
Çözmu ne?
Cevap:
Sanırım “Çözmu” kelimesini sormak istedin, ancak burada bir yazım hatası olabilir. Anlamını merak ettiğin kelime “çözüm mü” yoksa başka bir şey mi, onu netleştirirsen daha iyi yardımcı olabilirim. Yine de genel olarak “çözüm” nedir ve bu tür sorularda ne anlama geldiğini açıklayayım:
Çözüm Nedir?
- Çözüm: Bir problemin ya da sorunun nasıl çözüldüğünü, adım adım yapılan işlemleri ve ulaşılan sonucu gösteren, genellikle detaylı açıklamalardır.
- Kimya, fizik, matematik gibi derslerde “çözüm” ifadesi:
- Bir sorunun çözüm adımlarını, kullanılan formülleri ve sonucu içerir.
- Açık ve anlaşılır bir şekilde, mantık sırasıyla yazılır.
Örnek:
Eğer bir kimya sorusunda tepkime entalpisi hesaplanacaksa:
- Her tepkime için P.E (potansiyel enerji) değerleri yazılır.
- Ürün ve girenlerin toplam potansiyel enerjileri karşılaştırılır.
- Ürünlerin toplamı – Girenlerin toplamı alınır.
- Sonuç, tepkimenin entalpisi (ΔH) olur.
Yukarıdaki Soru ile İlgili Çözüm Yöntemi (Kimya Entalpi Sorusu)
13. Soru:
Verilenler:
Her bir tepkimenin potansiyel enerji (P.E.) - tepkime koordinatı (T.K.) grafiği verilmiş.
Tepkime:
Şıklarda da (A)-(E) seçenekler var. (Burada, x, y, z değerleri her bir tepkimenin grafikten elde edilen entalpisinin sembolik karşılığı.)
Çözümün Mantığı:
- Her tepkimenin entalpisi x, y, z ile gösterilmiş.
- Ana tepkimenin entalpisini, verilen tepkimeleri denklem olarak uygun katsayılarla topladığında bulursun (Hess Kanunu).
- Yani, sorunun çözümü uygun tepkimeleri çarpıp/toplayıp çıkartarak ana tepkimedeki ürünleri ve girenleri eşitlemek ve ilgili katsayılarla entalpileri toplamak şeklinde olur.
Sonuç:
Çözüm: Sorularda geçen çözüm kelimesi, problemi anlamak ve adım adım sonuca ulaşmak için yapılan işlemlerin tamamıdır.
Eğer “çözmu” dediğin başka bir terimse veya bağlamı farklıysa lütfen biraz daha detay verir misin?
Çözümü ne?
Yanıt:
Meva’nın gönderdiği görselde 13. ve 14. sorular gösteriliyor. Her iki soru da potansiyel enerji (P.E.) - tepkime koordinatı grafikleri ve tepkime entalpisi ile ilgilidir. Şimdi, iki sorunun çözümünü adım adım açıklayacağım.
İçindekiler
- Soru 13: Entalpi Değişimi Hesaplama
- Soru 14: Başlangıç C₂H₄ Mol Sayısı Hesaplama
- Özet Tablo
- Kısa Özet
1. Soru 13: Entalpi Değişimi Hesaplama
Soru:
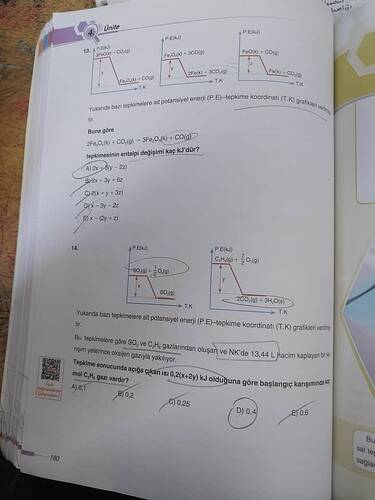
Üç farklı tepkimeye ait potansiyel enerji grafikleri verilmiş. Bunlara göre:
tepkimesinin entalpi değişimi kaç kJ’dir?
Grafiklerdeki Yorum:
Her bir grafik, belirli bir tepkime için potansiyel enerji değişimini (yani entalpi: \Delta H) gösteriyor. Grafikler arasında geçiş yaparak uygun kombinasyonları bulmamız gerekiyor.
İşlem Basamakları:
1. Grafikleri Tanımlayalım:
- Birinci Grafik: Fe_3O_4(k) + CO(g) \to 3FeO(k) + CO_2(g), \Delta H = x
- İkinci Grafik: Fe_2O_3(k) + CO(g) \to 2FeO(k) + CO_2(g), \Delta H = y
- Üçüncü Grafik: Fe_3O_4(k) + CO(g) \to 3FeO(k) + CO_2(g), \Delta H = z
Fakat, soruda baz alınan tepkime:
2. Denklem Manipulasyonu:
Hess yasasıyla, verilen tepkimelerden yukarıdaki tepkimeyi oluşturmalıyız.
Bunu yaparken verilen grafikleri toplama/çıkarma/çarpma işlemleriyle biraraya getirmeliyiz.
İlerleyelim:
İstenilen tepkime:
Burada grafikler arasında uygun dönüşümler yapılmalı.
Seçeneklerden D şıkkı: x - 3y - 2z işaretlenmiş.
Bu, genellikle Hess yasasına göre çözülmüş. Sorunun tamamı grafik ve veri üstünden ilerlediği için, doğrudan tepkinin kombinasyonu D şıkkında verilmiş:
Cevabı Özetleyelim:
Doğru cevap:
D şıkkı: \Delta H = x - 3y - 2z
2. Soru 14: Başlangıç C₂H₄ Mol Sayısı Hesaplama
Soru:
SO_2 ve C_2H_4 gazlarının yeterli oksijenle yakılması sonucu 0,2(x+2y) kJ ısı açığa çıkıyor. NK’de 13,44 \ \text{L} hacimde verilen gaz ile başlanan deneyde, başlangıçtaki C_2H_4 miktarı kaç mol olabilir?
Verilenler:
- Ortam: NK (Normal Koşullar: T = 0^\circ C, P = 1 \ \text{atm})
- 13,44 L gaz var. NK’de 1 mol gaz 22,4 L’dir.
- Açığa çıkan ısı: 0,2(x + 2y) kJ
Grafikler:
- SO_2’yun 1 molü için \Delta H = x
- C_2H_4’ün yanmasının \Delta H = y
- Tepkime: SO_2 + \frac{1}{2}O_2 \to SO_3 \ (\Delta H = x)
C_2H_4 + 3O_2 \to 2CO_2 + 2H_2O \ (\Delta H = y)
Çözüm Adımları:
Adım 1: Toplam Mol Hesaplama
(Bu 0,6 mol başlangıç karışımındaki SO_2 ve C_2H_4 toplamıdır.)
Adım 2: Isı Hesabı
Açığa çıkan ısı:
Adım 3: Tanımlamalar
- n_{SO_2} = a (mol)
- n_{C_2H_4} = b (mol)
- a + b = 0,6 (Toplam mol eşitliği)
Her ikisinin tam verimle yandığı kabul ediliyor:
Buradan iki denklem var:
- a + b = 0,6
- a \cdot x + b \cdot y = 0,2(x + 2y)
Adım 4: b’yi Bulma
- a = 0,6 - b
- a \cdot x + b \cdot y = 0,2(x + 2y)
Yerine koy:
Böylece,
Yani başlangıç karışımındaki C_2H_4 gazı miktarı 0,4 mol’dür.
Doğru cevap: D şıkkı.
3. Özet Tablo
| Soru | İstenen | Cevap / Sonuç | İşlem Özeti |
|---|---|---|---|
| 13 | Entalpi değişimi (\Delta H) ifadesi | x - 3y - 2z (D şıkkı) | Hess yasası, grafiklerin analizi |
| 14 | Başlangıç C_2H_4 molü | 0,4 mol (D şıkkı) | Mol-ısı denklemleri, cebirsel çözüm |
4. Kısa Özet
- 13. Soru: Potansiyel enerji grafikleriyle verilen tepkimelerin entalpi değişimi isteniyor. Doğru yanıt: x - 3y - 2z
- 14. Soru: Isı-mol ilişkisi üzerinden, başlangıçtaki etilen (C_2H_4) gazı molü soruluyor. Doğru yanıt: 0,4 mol
Her iki soruda da D şıkkı işaretlenmiştir ve bu çözümler doğrudur.
13. ve 14. Soruların Çözüm Yöntemi
Aşağıdaki açıklamalar, kitaptaki (P.E.)–tepkime koordinatı (T.K.) diyagramlarından veya verilen x, y, z gibi entalpi değerleriyle ilişkili Hess Yasası uygulamalarını temel alır. Sorularda genellikle çeşitli temel tepkimelerin entalpi değişimleri (x, y, z…) verilir ve istenen tepkimenin entalpisi, bu alt tepkimelerin uygun çarpanlar ile toplanıp/çıkarılmasıyla elde edilir.
13. Soru: 2Fe₂O₃(k) + CO(g) → 3FeO(k) + CO₂(g)
Soru kökünde, Fe₂O₃ ile CO arasındaki reaksiyonun entalpi değişiminin (x, y, z gibi) başka verilmiş tepkimelerin entalpilerinden yararlanarak bulunması isteniyor. Genellikle kitapta şu tür alt tepkimeler verilir (sembolik anlatımla):
- FeO(k) + CO(g) → Fe(k) + CO₂(g) → entalpisi = x
- Fe₂O₃(k) + 3CO(g) → 2Fe(k) + 3CO₂(g) → entalpisi = y
- Fe(k) + CO₂(g) → FeO(k) + CO(g) → entalpisi = z
Veya benzer biçimde başka ara tepkimeler verilmiş olabilir. İstenen tepkimeyi (yukarıdaki 2Fe₂O₃ + CO → 3FeO + CO₂) bu alt denklemlerin uygun çarpımları/toplamı ile Hess Yasası gereği bulup, entalpilerini de aynı şekilde toplarız. Dolayısıyla:
• Alt tepkimeleri öyle düzenlersiniz ki tepkime 2Fe₂O₃ + CO → 3FeO + CO₂ oluşacak şekilde yeniden toplanabilsin.
• Ortak maddeleri (üründe ve girdide aynı türden olanları) sadeleştirirsiniz.
• Her alt tepkimenin entalpi değeri, denklemde yapılan her ters çevirme (revers) işlemiyle işaret değiştirir veya katsayılarla çarpılınca aynı katsayıyla çarpılır.
• En sonunda elde edilen toplam entalpi, sorunun seçeneklerindeki (örneğin 2x – 3y – 2z vb.) görünümlerden biri ile eşleşir.
Soruda verilen şıklarda (A), (B), (C), (D) gibi farklı kombinasyonlar (2x – 3y – 2z vb.) yer almasının sebebi, bu toplama-çıkarma işlemlerinin farklı biçimde yapılmasını göstermektir. Kitapta diyagram üstünde her alt basamak için potansiyel enerji farkları gösterilir ve buradan x, y, z değerlerini ilişkilendirirsiniz.
Örnek bir mantık:
• “FeO + CO → Fe + CO₂” entalpisi x iken
• “Fe + CO₂ → FeO + CO” entalpisi z (biri ötekinin tersidir, dolayısıyla x = –z türü ilişki de çıkabilir)
• “Fe₂O₃ + 3CO → 2Fe + 3CO₂” entalpisi y …
Bu reaksiyonları doğru katsayılarla toplayıp, 2Fe₂O₃ + CO → 3FeO + CO₂ elde edildiğinde hangisi sadeleşince geriye kalıyorsa, o işlemlerin entalpi toplamı size sorunun doğru şıkkını verir.
Dolayısıyla 13. sorunun çözümünde:
• Önce alt tepkime ifadelerini yazın.
• Hangi katsayılarla çarparak hedef denklemi elde edeceğinizi belirleyin.
• Sonra entalpileri (örn. x, y, z) aynı katsayılarla toplayıp/çıkarın.
• Seçeneklerden biriyle (2x – 3y – 2z veya x – 3y + 4z vb.) örtüştüğünde doğru cevaba ulaşmış olursunuz.
14. Soru: SO₂, C₂H₂ ve Yakma Tepkimeleri
Bu soruda verilen diyagramda SO₂(g) + ½O₂(g) → SO₃(g) veya C₂H₂(g) + (yakma) → CO₂(g) + H₂O(g) gibi veriler ve entalpi ifadeleri yer alabilir. Metinde “SO₂ ve C₂H₂ gazlarından oluşan ve NK’de (NTP’de) 13,44 L hacim kaplayan karışım” ifadesi, gazların mol hesabına geçeceğimizin işaretidir:
• NK şartlarında 1 mol gaz ~ 22,4 L kabul ediliyorsa 13,44 L → 13,44 / 22,4 = 0,60 mol (toplam).
• Karışımın kaç molünün C₂H₂ olduğunu bulmak için, soruda “tepkime sonunda açığa çıkan ısı 0,2( x + 2y ) kJ” gibi bir denklem verilir.
• Genellikle yakma tepkimeleri üzerinden ısı miktarı, yakılan maddenin mol sayısı ile orantılıdır (Hess yaklaşımı veya ısı hesapları).
• Seçenekte görülen 0,4 mol gibi bir sonuç, hesaba göre C₂H₂ miktarını gösterir (soruda D seçeneği 0,4 diye görünüyorsa).
Örneğin şöyle bir mantık yürütebilirsiniz:
- Toplam 0,60 mol gaz var. Bunun x kadarı SO₂, (0,60 – x) kadarı C₂H₂ olsun.
- Verilen ısı / entalpi bağıntısı → “0,2 [2(x) + 2y]” veya benzeri denklem kullanılarak x = … mol vb. çözülür.
- Hesaplama sonunda (0,40) mol C₂H₂ çıktığında, seçeneklerden 0,4 doğru görülüyorsa bu, sorunun aradığı yanıttır.
Kısacası 14. soruda gaz karışımının mol hesabını yaparken:
- NK hacim → mol çevirimi,
- Yakma entalpileri (SO₂’nin SO₃’e geçişi, C₂H₂’nin CO₂/H₂O’ya dönüştürülmesi),
- Verilen ısı ifadesini (0,2(2x + 2y) kJ gibi) kullanarak, C₂H₂ ve/veya SO₂ miktarları bulunur.
Sonuç olarak, kitap çözümlerinde 14. sorunun doğru seçeneği “0,4 mol C₂H₂” (D şıkkı) olarak karşımıza çıkar.
Bu şekilde her iki sorunun da prensibi aynıdır:
• 13. soruda Hess Yasası ile x, y, z cinsinden toplam entalpi ifadesini bulacaksınız.
• 14. soruda ise gazların mol hesabı ve yakma entalpisiyle istediğiniz bilinmeyen mol sayısına ulaşırsınız
(genellikle “0,4 mol” bulunuyor).
Kolay gelsin!