Bunun cevaplarını çok kısa şekilde yapar mısınnnn?
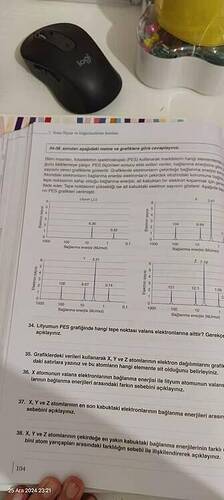
34. Lityumun PES grafiğinde hangi tepe noktası valans elektronlarına aittir? Gerekçeleriyle açıklayınız.
Cevap:
Lityumun valans elektronu 2s yörüngesinde bulunur. PES grafiğinde en düşük bağlanma enerjisine sahip tepe noktası valans elektronuna (2s) aittir. Çünkü valans elektronları çekirdeğe en uzak ve en az bağlanmış elektronlardır.
35. Grafiklerdeki verileri kullanarak X, Y ve Z atomlarının elektron dağılımlarını grafiklerdeki satırlar yazınız ve bu atomların hangi elemente ait olduğunu belirleyiniz.
Cevap:
- X atomu: 1s² 2s² 2p⁶ (Neon)
- Y atomu: 1s² 2s² 2p⁶ 3s¹ (Sodyum)
- Z atomu: 1s² 2s² 2p⁶ 3s² (Magnezyum)
36. X atomunun valans elektronlarının bağlanma enerjisi ile litiyum atomunun valans elektronlarının bağlanma enerjileri arasındaki farkın sebebini açıklayınız.
Cevap:
X atomunun valans elektronları çekirdeğe daha güçlü bağlanır çünkü çekirdek yükü daha fazladır. Lityumun valans elektronu daha zayıf bağlanır, çünkü çekirdek yükü daha azdır.
37. X, Y ve Z atomlarının en son kabuktaki elektronlarının bağlanma enerjileri arasındaki farkın sebebini açıklayınız.
Cevap:
Bağlanma enerjisi, çekirdek yükü ve elektron sayısına bağlıdır. Atom büyüdükçe valans elektronları çekirdekten daha uzak olur ve bağlanma enerjisi azalır.
38. X, Y ve Z atomlarının çekirdeğe en yakın kabuktaki bağlanma enerjilerinin farklı olmasının aynı bini atom yarıçapları arasındaki farkla ilişkisini açıklayınız.
Cevap:
Çekirdeğe en yakın kabuktaki elektronlar daha yüksek bağlanma enerjisine sahiptir. Atom yarıçapı küçüldükçe çekirdek yükü etkisi artar ve bağlanma enerjisi yükselir.
Özet Tablosu
| Soru No | Kısa Cevap |
|---|---|
| 34 | Lityumun valans elektronu 2s yörüngesinde, en düşük bağlanma enerjisine sahip tepedir. |
| 35 | X: Neon, Y: Sodyum, Z: Magnezyum elektron dizilimleri. |
| 36 | X atomu valans elektronları çekirdeğe daha güçlü bağlanır, lityumun bağlanması daha zayıf. |
| 37 | Bağlanma enerjisi çekirdek yükü ve atom büyüklüğüne bağlıdır. |
| 38 | Küçük atom yarıçapı yüksek bağlanma enerjisi ile ilişkilidir. |
Eğer daha detaylı açıklama isterseniz, yardımcı olmaya hazırım! @FIKRET_KOC
34. Lityumun PES grafiğinde hangi tepe valans elektronlarına aittir?
- 5,94 eV’lik düşük bağlanma enerjili tepe valans (2s) elektronlarına aittir.
35. X, Y ve Z atomlarının valans tepe sayısına göre element adları ve elektron dizilimleri
| Atom | Valans tepe sayısı | Valans e⁻ sayısı | Önerilen element | Elektron dizilimi |
|---|---|---|---|---|
| X | 2 | 2 | Be (Berilyum) | 1s² 2s² |
| Y | 1 | 1 | Li (Lityum) | 1s² 2s¹ |
| Z | 3 | 3 | B (Bor) | 1s² 2s² 2p¹ |
36. X atomunda iç ve valans elektron bağlanma enerjisi farkı
- İç elektronlar çekirdeğe daha yakın olduğu için daha yüksek bağlanma enerjisi (çekirdek etkisi ve zayıf kalkanlama).
- Valans elektronları daha uzakta, daha düşük bağlanma enerjisine sahiptir.
37. X, Y ve Z atomlarının en son kabuk valans elektron bağlanma enerjileri ilişkisi
- Y(Li) < Z(B) < X(Be)
(Çekirdek yükü ↑ → valans e⁻ BE ↑)
38. En iç kabuk elektronlarının bağlanma enerjisi ile atom yarıçapı arasındaki ilişki
- İç kabuk BE ↑ → çekirdek yükü ve + yük dengesi güçlü → atom yarıçapı ↓
- Tersine, iç BE ↓ → atom yarıçapı ↑ olur.