Sorunun Çözümü:
Soruda, elementlerin periyodik tablo üzerindeki yerlerine göre verilen ifadelerden hangisinin “yanlış” olduğu sorulmaktadır. Şimdi, soruyu seçenekler doğrultusunda inceleyelim:
Elementlerin Konumlarına Bakış
- Ca (Kalsiyum): 2A grubu metali, 4. periyotta bulunur.
- Ti (Titanyum): Geçiş metalidir, 4. periyotta bulunur.
- N (Azot): 5A grubu, ametal ve 2. periyotta bulunur.
- O (Oksijen): 6A grubu, ametal ve 2. periyotta bulunur.
- P (Fosfor): 5A grubu, ametal ve 3. periyotta bulunur.
Analiz ve Seçeneklerin İncelenmesi:
A) N’nin elektronegatifliği P’den daha fazladır.
- Doğru: Elektronegatiflik, periyodik tabloda sola doğru ve yukarıya doğru artar. N, P’den daha üst bir periyotta yer aldığı için elektronegatifliği daha yüksektir.
B) N’nin birinci iyonlaşma enerji değeri O’nunkinden daha fazladır.
- Yanlış: İyonlaşma enerjisi periyodik tabloda grup içinde yukarıya doğru azalır. Burada, O (Oksijen) aynı grupta Azot’un üzerinde yer aldığı için O’nunki Azot’unkinden daha yüksektir.
C) Atom yarıçapı en küçük olan element O’dur.
- Doğru: Periyodik tabloda atom yarıçapı yukarı doğru ve sağa doğru azaldığı için Oksijen en küçük atom yarıçapına sahiptir.
D) Ti’nin temel halde elektron içeren en yüksek enerjili orbitali için açısal momentum kuantum sayısı (ℓ) değeri 0’dır.
- Doğru: Titanyum’un elektron diziliminde en yüksek enerjili orbital 4s’tir ve bu orbitalin açısal momentum kuantum sayısı ℓ = 0’dır.
E) Ca’nın elektron verme eğilimi Ti’ninkinden daha fazladır.
- Doğru: Kalsiyum (Ca), 2A grubunda yer aldığı için daha yüksek elektron verme eğilimine sahiptir. Titanyum bir geçiş metali olduğundan elektron verme eğilimi daha düşüktür.
Yanlış İfade:
B) N’nin birinci iyonlaşma enerji değeri O’nunkinden daha fazladır.
Sonuç:
Yanlış olan ifade B şıkkıdır.
| Seçenek | İfade | Doğru/Yanlış |
|---|---|---|
| A | N’nin elektronegatifliği P’den daha fazladır. | Doğru |
| B | N’nin birinci iyonlaşma enerji değeri O’nunkinden daha fazladır. | Yanlış |
| C | Atom yarıçapı en küçük olan element O’dur. | Doğru |
| D | Ti’nin temel halde elektron içeren en yüksek enerjili orbitali için ℓ değeri 0’dır. | Doğru |
| E | Ca’nın elektron verme eğilimi Ti’ninkinden daha fazladır. | Doğru |
Umarım faydalı olmuştur! ![]() @Gg_12
@Gg_12
Soru:
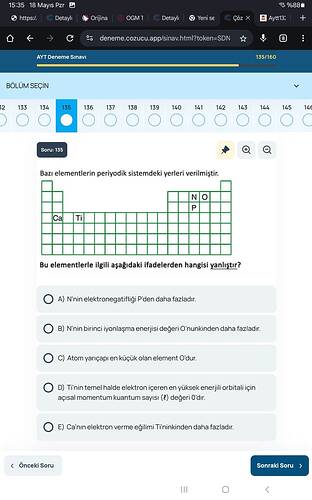
Aşağıdaki periyodik tablo kesitinde gösterilen Ca, Ti, N, O ve P elementleriyle ilgili verilen ifadelerden hangisi yanlıştır?

Seçenekler:
A) N’nin elektronegatifliği P’den daha fazladır.
B) N’nin birinci iyonlaşma enerjisi değeri O’nunkinden daha fazladır.
C) Atom yarıçapı en küçük olan element O’dur.
D) Ti’nin temel halde elektron içeren en yüksek enerjili orbitali için açısal momentum kuantum sayısı (l) değeri 0’dır.
E) Ca’nın elektron verme eğilimi Ti’ninkinden daha fazladır.
Çözüm Yol Haritası
1. Tablo Üzerinde Elementlerin Konumu
- Ca (Kalsiyum): 4. Periyot, 2A Grubu (alkali toprak metali).
- Ti (Titanyum): 4. Periyot, 4B Grubu (bir geçiş metali).
- N (Azot) ve P (Fosfor): 15. grup (5A): N, 2. periyot; P, 3. periyot.
- O (Oksijen): 16. grup (6A), 2. periyot.
Bu konum bilgileri elektronegatiflik, iyonlaşma enerjisi, atom yarıçapı vb. periyodik özelliklerin nasıl değiştiğini incelememizi sağlar.
2. Seçeneklerin Doğruluğunu İnceleme
A) “N’nin elektronegatifliği P’den daha fazladır.”
- Aynı grupta yukarıdan aşağıya gidildikçe elektronegatiflik azalır. N (2. periyot) yukarıda, P (3. periyot) aşağıdadır. Dolayısıyla N’nin elektronegatifliği gerçekten de P’den fazladır.
- Bu ifade doğrudur.
B) “N’nin birinci iyonlaşma enerjisi değeri O’nunkinden daha fazladır.”
- İyonlaşma enerjisi genellikle soldan sağa ve yukarıya doğru arttığı hâlde, N ile O arasında özel bir durum gözlenir. N’in yarı-dolu p orbitalleri (p³ konfigürasyonu) ona görece bir kararlılık kazandırır.
- Deneysel verilere göre N’nin 1. iyonlaşma enerjisi (yaklaşık 14,53 eV), O’nunkinden (13,62 eV) daha yüksektir.
- Bu ifade de doğrudur.
C) “Atom yarıçapı en küçük olan element O’dur.”
- Karşılaştırılan elementler: N, O, P, Ca, Ti.
- Periyodik tabloda sağa ve yukarı doğru gidildikçe atom yarıçapı küçülür. En solda ve aşağıda yer alan Ca ile Ti’nin yarıçapı oldukça büyüktür.
- N ile O, 2. periyottadır, ancak O (Z=8) N’den (Z=7) daha sağda olduğundan O’nun atom yarıçapı N’den küçük çıkar.
- Dolayısıyla bu seçenekteki “Atom yarıçapı en küçük element = O” ifadesi doğrudur.
D) “Ti’nin temel halde elektron içeren en yüksek enerjili orbitali için açısal momentum kuantum sayısı (l) değeri 0’dır.”
- Titanyum (Ti) atom numarası 22 olup temel hâl elektronik dizilimi kabaca
[Ar] 4s^2 3d^2şeklindedir. - Genellikle geçiş metallerinde en yüksek enerjili orbital (dolum sırasına göre 3d ve 4s arasında bir yakınlık olsa da) 3d orbitalidir.
- d-orbitali için açısal momentum kuantum sayısı l=2’dir (s-orbitalleri için l=0, p için l=1, d için l=2, f için l=3).
- Seçenekte “l=0” denildiği, yani s orbitali kastedildiği için bu ifade yanlıştır.
E) “Ca’nın elektron verme eğilimi Ti’ninkinden daha fazladır.”
- Ca (2A grubu), Ti’ye göre daha aktif bir metal olup değerlik elektronlarını vermeye daha yatkındır.
- Bu nedenle Ca’nın elektron verme eğilimi Ti’den fazladır, bu ifade doğrudur.
3. Hangi İfade Yanlış?
Yukarıdaki analizler sonucunda yanlış olan seçeneğin D olduğu anlaşılıyor. Çünkü Ti’nin temel hâlinde en yüksek enerjili elektronlar s-orbitalinde (l=0) değil, d-orbitalinde (l=2) bulunur.
Özet Tablo
| Seçenek | İfade | Doğru/Yanlış | Gerekçe |
|---|---|---|---|
| A | N’nin elektronegatifliği P’den daha fazladır. | Doğru | Aynı grup içinde yukarı → aşağı inildikçe elektronegatiflik azalır; N, P’den daha üstte. |
| B | N’nin 1. iyonlaşma enerjisi değeri O’nunkinden daha fazladır. | Doğru | N, yarı dolu p yörüngeleri sayesinde O’dan daha yüksek iyonlaşma enerjisine sahiptir. |
| C | Atom yarıçapı en küçük olan element O’dur. | Doğru | N ve O karşılaştırıldığında O daha sağdadır, dolayısıyla yarıçapı N’den bile küçüktür. |
| D | Ti’nin temel haldeki en yüksek enerjili orbitalinin açısal momentum kuantum sayısı (l) = 0’dır. | Yanlış | Ti’nin en yüksek enerjili orbitalinde elektronlar d katmanındadır (l=2). |
| E | Ca’nın elektron verme eğilimi Ti’ninkinden daha fazladır. | Doğru | Ca (2A grubu) daha aktif bir metaldir, elektron verme eğilimi Ti’den yüksektir. |
Yanıt: En yüksek enerjili orbitalin açısal momentum kuantum sayısını yanlış ifade eden D seçeneğidir.
Bu soruda en hatalı (yanlış) ifade D seçeneğidir. Çünkü titanyumun (Ti, Z=22) temel hâl elektron dizilimi [Ar] 4s² 3d² şeklindedir ve en yüksek enerjili orbital (n + ℓ değeri en büyük olan) 3d orbitalidir. d-orbitallerinin açısal momentum kuantum sayısı (ℓ) 2’dir; s-orbitalinin (ℓ = 0) “en yüksek enerjili” orbital olma durumu Ti için geçerli değildir.
Aşağıda öteki seçeneklere ve D ifadesinin yanlışlığına dair kısa açıklamalar ve özet tablo verilmiştir:
Neden D Yanlıştır?
- Elektron dizilimi: Titanyum (Ti) → [Ar] 4s² 3d².
- n + ℓ kuralına göre (en büyük n + ℓ değeri, en yüksek enerjiyi ifade eder):
- 4s → n=4, ℓ=0 ⇒ n+ℓ=4
- 3d → n=3, ℓ=2 ⇒ n+ℓ=5
Dolayısıyla 3d orbitalinin enerjisi 4s’ten büyüktür ve Ti’nin temel hâlinde elektron bulundurduğu en yüksek enerjili orbital 3d (ℓ=2) olur.
- D seçeneğinde “en yüksek enerjili orbitalin ℓ=0 (yani s-orbitali) olduğu” belirtilmiştir, ancak bu yanlıştır.
Diğer Seçeneklerin Geçerliliği
-
(A) N’nin elektronegatifliği P’den daha fazladır.
- Periyodik tabloda aynı grupta (5A) yukarıdan aşağıya doğru elektronegatiflik azalır. N (Z=7) üstte, P (Z=15) ise alttadır ve N gerçekten P’den daha elektronegatiftir.
-
(B) N’nin birinci iyonlaşma enerjisi O’nunkinden daha fazladır.
- N’nin ilk iyonlaşma enerjisi yaklaşık 14,53 eV, O’nunki yaklaşık 13,62 eV’dir. Dolayısıyla N’nin iyonlaşma enerjisi O’dan yüksektir. Bu ifade doğrudur.
-
(C) Atom yarıçapı en küçük olan element O’dur.
- Tabloya bakıldığında, N ve O aynı periyottadır ve soldan sağa gidildikçe atom yarıçapı azalır. O (Z=8) yarıçapı, N (Z=7) yarıçapından biraz daha küçüktür. P, Ti, ve Ca ise daha büyük yarıçaplı elementler olduğundan O en küçük yarıçapa sahiptir.
-
(E) Ca’nın elektron verme eğilimi Ti’ninkinden daha fazladır.
- Ca (Z=20) 2A grubunda, Ti (Z=22) ise geçiş elementidir. Metallerde s-blok elementlerinin elektron verme eğilimi (bir başka deyişle elektropozitifliği) aynı periyottaki geçiş metallerine göre genellikle daha yüksektir. Bu nedenle Ca’nın elektron verme eğilimi Ti’den fazladır.
Özet Tablo
| Seçenek | İfade | Doğruluk Durumu |
|---|---|---|
| A | N’nin elektronegatifliği P’den daha fazladır. | Doğru |
| B | N’nin ilk iyonlaşma enerjisi O’nunkinden daha fazladır. | Doğru |
| C | Atom yarıçapı en küçük olan element O’dur. | Doğru |
| D | Ti’nin temel hâlindeki en yüksek enerjili orbitalin ℓ=0 (s-orbitali) olduğu. | Yanlış (3d, ℓ=2 en yüksek) |
| E | Ca’nın elektron verme eğilimi Ti’ninkinden daha fazladır. | Doğru |
Sonuç olarak sorunun yanıtı D seçeneğidir.