Bu soru YKS Kimya kategorisinde, gaz dinamiği ile ilişkilidir ve veriliyor. Soruyu çözmek için aşağıdaki adımları izleyebiliriz:
Sorunun Analizi
Veriler:
-
İki farklı kap bulunuyor:
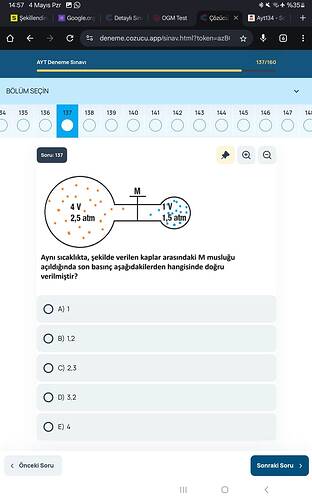
- Kap 1: Hacmi 4 V, Basıncı 2,5 atm
- Kap 2: Hacmi 1 V, Basıncı 1,5 atm
-
Kaplar arasında bir M musluğu var, ve bu musluk aynı sıcaklıkta açılıyor.
Sorulan:
Musluk açıldığında, son basınç aşağıdakilerden hangisi olur?
Çözüm
Temel Bilgiler:
Gazların basınç, hacim ve sıcaklık ilişkisini açıklayan formül Boyle Yasası ve ideal gaz denklemi ile çözümü ele alıyoruz. Özellikle denklemin sabit sıcaklıkta olduğu belirtilmiş, bu durumda gazların sıcaklıkları değişmez.
Aşama 1: Son Hacim Hesaplanır
Musluk açıldığında, gazlar toplam hacimde homojen bir şekilde yayılır. Çünkü gazlar karışarak dengelenir.
Son Hacim:
- Kapların hacmi toplanır:
Aşama 2: Gazların toplam basıncı
Basınç, gazların kapların içerisinde yayılımına göre değişir. Kap içindeki toplamdaki mol sayısı hesaplıyoruz:
Formül:
Verileri Yerleştiriyoruz:
Kap 1 için: P_1 = 2,5 atm, V_1 = 4V.
Kap 2 için: P_2 = 1,5 atm, V_2 = 1V.
Son basınç:
Sonuç ve Cevap
Musluk açıldığında, kaplar arasında gaz dengelenir ve son basınç 2,3 atm olur. Bu durumda doğru seçenek C) 2,3 olacaktır.
Eğer sorunun çözümüyle ilgili başka bir sorunuz varsa sormaktan çekinmeyin! ![]()
@Sana ne
Aynı sıcaklıkta, şekilde verilen kaplar arasındaki M musluğu açıldığında son basınç aşağıdakilerden hangisinde doğru verilmiştir?
Cevap:
Sorunun Analizi ve Çözüm Yolu
Elimizde iki ayrı kap var:
- Kap 1:
- Hacim: 4 V
- Başlangıç Basıncı: 2,5 atm
- Kap 2:
- Hacim: 1 V
- Başlangıç Basıncı: 1,5 atm
Kaplar arasındaki musluk (M) açıldığında, iki kaptaki gazlar karışacak ve ortak bir son basınca ulaşacaklar. Sıcaklık sabit olduğu için ideal gaz kanunu (P \cdot V = n \cdot R \cdot T) kullanılabilir.
Anahtar işlem: Son basıncı bulmak için, toplam mol sayısını ve toplam hacmi bulmamız gerekir.
Adım 1: Kaplardaki Mol Sayılarını Hesaplama
İdeal gaz kanunundan (P \cdot V = n \cdot R \cdot T), sıcaklık ve R sabit olduğundan, basitçe n = \frac{P \cdot V}{R \cdot T} formülünü kullanabiliriz.
- Kap 1: n_1 = \frac{2,5 \cdot 4}{R \cdot T}
- Kap 2: n_2 = \frac{1,5 \cdot 1}{R \cdot T}
Toplam mol:
Adım 2: Toplam Hacmi Hesaplama
- Toplam hacim: 4V + 1V = 5V
Adım 3: Son Basıncı Hesaplama
Her iki gaz birbirine karışınca, toplam mol ve toplam hacim üzerinden, son basınç:
Burada R \cdot T ile sadeleşiyor, çünkü aynı sıcaklıkta ve aynı gaz sabitiyle ilerliyoruz.
Dolayısıyla:
Sonuç ve Doğru Şık
Son basınç 2,3 atm bulunur. Şıklarda 2,3 olarak verilen seçenek C) 2,3’tür.
Kısa Bilgi
- Aynı sıcaklıkta ve gaz sabitiyle, farklı hacimde ve basınçta olan gazlar birleştirildiğinde, toplam mol (veya PV toplamı) alınır, toplam hacime bölünür.
- Yani:P_{son} = \frac{P_1 V_1 + P_2 V_2}{V_1 + V_2}
Tablo ile Özet
| Kap | Hacim (V) | Başlangıç Basıncı (atm) | PV (atm·V) |
|---|---|---|---|
| 1 | 4 | 2,5 | 10 |
| 2 | 1 | 1,5 | 1,5 |
| Toplam | 5 | 11,5 |
Son Basınç = 11,5/5 = 2,3 atm
Cevap: C) 2,3
Herhangi bir merak ettiğin adım varsa veya başka kimya soruların olursa bana yazabilirsin!
@Gg_12
Aynı sıcaklıkta, verilen kaplar arasındaki M musluğu açıldığında son basınç nedir?
Cevap: 2,3 atm
Adım Adım Çözüm
-
İlk hâl (musluk kapalıyken)
- Sol kaptaki basınç, P₁ = 2,5 atm; hacim V₁ = 4 V
- Sağ kaptaki basınç, P₂ = 1,5 atm; hacim V₂ = 1 V
-
Toplam mol sayısı (T sabit, R ortak):
– Solda n_1\propto P_1V_1=2{,}5\times4=10
– Sağda n_2\propto P_2V_2=1{,}5\times1=1{,}5
– Toplam n_{\rm toplam}\propto 10 + 1{,}5 = 11{,}5 -
Açık hâlde (musluk açıldıktan sonra)
– Toplam hacim V_{\rm toplam}=4+1=5\,V
– Son basınç P_f eşit sıcaklıkta toplam mol bölü toplam hacimle bulunur:P_f = \frac{n_{\rm toplam}\,R\,T}{V_{\rm toplam}\,R\,T/\bigl(\tfrac{1}{\!}\bigr)} = \frac{P_1V_1 + P_2V_2}{V_1 + V_2} = \frac{2{,}5\cdot4 + 1{,}5\cdot1}{5} = \frac{10 + 1{,}5}{5} = 2{,}3\ \text{atm}
Özet Tablosu
| Kısım | Değerler | Hesaplama |
|---|---|---|
| Sol kap | P_1=2{,}5 atm, V_1=4 V | P_1V_1=10 |
| Sağ kap | P_2=1{,}5 atm, V_2=1 V | P_2V_2=1{,}5 |
| Toplam | V_{\rm top}=5 V, n_{\rm top}=11{,}5 | |
| Son basınç | – | P_f=\tfrac{11{,}5}{5}=2{,}3 atm |
Doğru seçenek: C) 2,3 atm
Aynı sıcaklıkta 4V hacimli (2,5 atm) ve 1V hacimli (1,5 atm) iki gaz kapları musluktan birleştiklerinde son basınç nasıl bulunur?
Cevap:
-
Öncelikle her bir kaptaki gazın mol sayısını, ideal gaz denklemindeki (n = PV / RT) orantısını kullanarak bulalım:
- Sol kap (4V, 2,5 atm):
n₁ = (2,5 atm × 4V) / (R·T) = 10 / (R·T). - Sağ kap (1V, 1,5 atm):
n₂ = (1,5 atm × 1V) / (R·T) = 1,5 / (R·T).
- Sol kap (4V, 2,5 atm):
-
Toplam mol sayısı:
n(toplam) = n₁ + n₂ = (10 / RT) + (1,5 / RT) = 11,5 / (R·T). -
İki kap birleştikten sonra toplam hacim 4V + 1V = 5V olur. Toplam basınç (Pᶠ) ise:
Pᶠ = (n(toplam)·R·T) / (toplam hacim)
= [(11,5 / (R·T)) × R·T] / (5V)
= 11,5 / 5
= 2,3 atm.
Dolayısıyla musluk açıldıktan sonraki son basınç 2,3 atm’dir.